题目内容
1.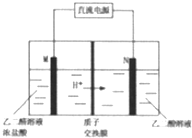 乙醛酸(HOOC-CHO)是有机合成的重要中间体.工业上用“双极室成对电解法”生产乙醛酸,原理如图所示.该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸.下列说法不正确的是( )
乙醛酸(HOOC-CHO)是有机合成的重要中间体.工业上用“双极室成对电解法”生产乙醛酸,原理如图所示.该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸.下列说法不正确的是( )| A. | N电极上的电极反应式:HOOC-COOH+2e-+2H+═HOOC-CH0+H2O | |
| B. | 若有2molH+通过质子交换膜并完全参与反应,则该装置中生成的乙醛酸为1mol | |
| C. | M电极上的电极反应式为:2Cl--2e-═Cl2↑ | |
| D. | 乙二醛与M电极的产物反应生成乙醛酸的化学方程式:Cl2+OHC-CHO+H2O═HOOC-CHO+2HCl |
分析 A、N电极上HOOC-COOH得电子生成HOOC-CHO;
B、2mol H+通过质子交换膜,则电池中转移2mol电子,根据电极方程式计算;
C、根据质子的移动方向,确定M电极是阳极,阳极上发生失电子的氧化反应;
D、氯气具有氧化性,能将醛基氧化为羧基,据此书写方程式即可.
解答 解:A、N电极上HOOC-COOH得电子生成HOOC-CHO,则电极反应式为HOOC-COOH+2e-+2H+═HOOC-CHO+H2O,故A正确;
B、2mol H+通过质子交换膜,则电池中转移2mol电子,根据电极方程式HOOC-COOH+2e-+2H+═HOOC-CHO+H2O,可知生成1mol乙醛酸,由于两极均有乙醛酸生成所以生成的乙醛酸为2mol,故B错误;
C、根据质子的移动方向,确定M电极是阳极,阳极上发生失电子的氧化反应:2Cl--2e-═Cl2↑,故C正确;
D、氯气具有氧化性,能将醛基氧化为羧基,乙二醛与M电极的产物反应生成乙醛酸的化学方程式为:Cl2+OHC-CHO+H2O═HOOC-CHO+2HCl,故D正确.
故选B.
点评 本题考查了电解池原理的分析应用,把握电解池原理以及电解过程中电子守恒的计算应用,掌握基础是关键,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
17.苯是重要的有机化工原料.下列关于苯的性质说法正确的是( )
| A. | 常温常压下为气体 | B. | 能发生氧化反应 | ||
| C. | 不能发生取代反应 | D. | 易溶于水 |
9.某有机物m g与过量钠反应生成V L气体.该有机物m g与过量小苏打反应,生成相同状况下的气体V L.则此有机物可能是下列中的( )
| A. | HO(CH2)2CHO | B. | HO(CH2)2COOH | C. | HOOCCOOH | D. | (CH3)3CCOOH |
16.短周期元素X、Y、Z、W、M的原子序数依次增大,X、Z同主族,Z、W、M同周期,其 中X与Y能形成两种物质,且常温下均为液体.W的氧化物既能溶于强碱溶液,又能溶于 X、M形成的水溶液.已知W与M形成的物质在178°C时升华.下列说法不正确的是( )
| A. | Z、W、M的原子半径由大到小的顺序为Z>W>M | |
| B. | M分别与Z、W所形成的物质的晶体类型相同 | |
| C. | X2Y2易溶于X2Y中,是由于X2Y2与X2Y能形成分子间氢键 | |
| D. | 将Z2Y在空气中加热可得到Z2Y2 |
6.日本的核泄漏引起了人们对核能的恐慌,也加剧了人类对化石燃料的依赖,化石燃料特别是煤的使用不会加剧环境污染,工业上常把煤进行汽化、液化处理,使煤变成清洁能源,煤的一种转化流程图如图:
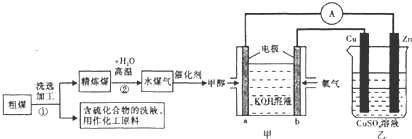
(1)随着反应的进行,乙池的电解质溶液的pH不变(填“增大、减小、不变”);甲池中负极的电极反应式为CH3OH-6e-+8OH-=CO32-+6H2O.
(2)已知在常温常压下:①CH3OH(l)+3O2(g)=2CO2(g)+4H2O△H=-1451.6kJ/mol
②2CO(g)+O2(g)=2CO2(g)△H=-566kJ/mol
则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H═-442.8kJ/mol.
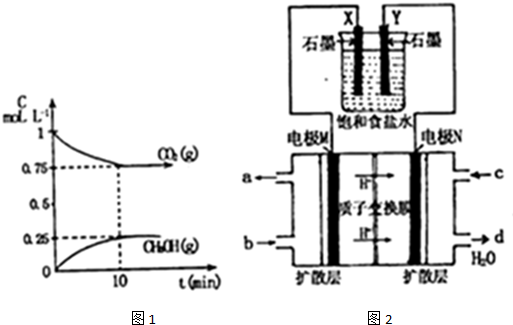
(3)C(s)和H2O(g)在一定条件下反应可得到H2等清洁燃料.将不同量的C(s)和H2O(g)分别加入到体积为2L的恒容密闭容器中发生反应:C(s)+H2O(g)?CO(g)+H2(g),不同温度下得到三组数据:
①实验2条件下平衡常数K=0.75;若实验2中分离出1molH2O(g),则H2O(g)的转化率将增大(填“增大、减小、不变”);
②若实验3起始时充入的是CO(g)和H2(g),且达平衡时实验2、3中CO的体积分数相同,则起始时c(H2)==1.5mol/L.

(1)随着反应的进行,乙池的电解质溶液的pH不变(填“增大、减小、不变”);甲池中负极的电极反应式为CH3OH-6e-+8OH-=CO32-+6H2O.
(2)已知在常温常压下:①CH3OH(l)+3O2(g)=2CO2(g)+4H2O△H=-1451.6kJ/mol
②2CO(g)+O2(g)=2CO2(g)△H=-566kJ/mol
则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为CH3OH(l)+O2(g)=CO(g)+2H2O(l)△H═-442.8kJ/mol.
(3)C(s)和H2O(g)在一定条件下反应可得到H2等清洁燃料.将不同量的C(s)和H2O(g)分别加入到体积为2L的恒容密闭容器中发生反应:C(s)+H2O(g)?CO(g)+H2(g),不同温度下得到三组数据:
| 实验组 | 温度/C | 起始量/mol | 平衡量/mol | 达平衡所需时间/min | ||
| C | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | … | 6 |
| 2 | 900 | 6 | 3 | … | 1.5 | 3 |
| 3 | 900 | … | … | … | … | 1 |
②若实验3起始时充入的是CO(g)和H2(g),且达平衡时实验2、3中CO的体积分数相同,则起始时c(H2)==1.5mol/L.
13.从下列实验事实所得出的相应结论正确的是( )
| 实验事实 | 结论 | |
| ① | 将某气体通入品红溶液中,品红溶液褪色 | 该气体一定是SO2 |
| ② | 将燃烧的镁条放入CO2中能继续燃烧 | 还原性:Mg>C |
| ③ | NaHCO3溶液与NaAlO2溶液混合产生白色沉淀 | 酸性:HCO3->Al(OH)3 |
| ④ | 常温下白磷自燃而氮气在放电时才与氧气反应 | 非金属性:P>N |
| ⑤ | 某无色溶液中加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝 | 该溶液一定有NH4+ |
| A. | ①②③ | B. | ①③⑤ | C. | ②③⑤ | D. | ③④⑤ |
11.下列有机物的命名正确的是( )
| A. | 2-乙基戊烷 | B. | 1,2-二甲基己烷 | ||
| C. | 2-甲基-4-乙基庚烷 | D. | 2,3-二乙基-4-甲基己烷 |