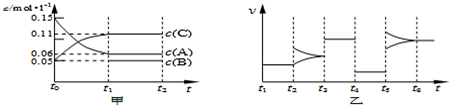题目内容
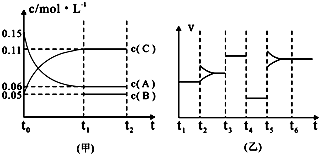
向某密闭容器中加入 0.3molA、0.1molC 和一定量的 B 三种气体.一定条件下发生反应,各物质浓度随时间变化如下图中甲图所示.附图中乙图为 t2时刻后改变容器中条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件,所用条件均不同.已知,t3~t4阶段为使用催化剂[已知t~t1阶段 c( B)未画出].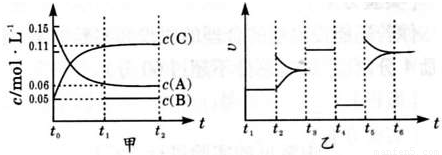
(1)若 t1=15s,则t~t1阶段以 C 浓度变化表示的反应速率为v( C )= .
(2)t4~t5阶段改变的条件为 ,B 的起始物质的量为 .
(3)t5~t6阶段容器内 A 的物质的量共减少 0.03mol,而此过程中容器与外界的热交换总量为 akJ,写出该反应的热化学方程式: .
【答案】分析:(1)根据v=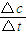 计算反应速率;
计算反应速率;
(2)t4~t5阶段正逆反应速率减小且相等,如是降低温度,平衡移动发生移动,则正逆反应速率不相等;
根据C、A浓度的变化判断二者计量数关系,根据t4~t5阶段判断化学方程式,根据化学方程式计算;
(3)计算3molA反应的热量,结合方程式书写热化学方程式.
解答:解:(1)若t1=15s,生成物C在t~t1时间段的平均反应速率为:v=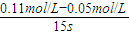 =0.004mol?L-1?s-1,故答案为:0.004mol?L-1?s-1;
=0.004mol?L-1?s-1,故答案为:0.004mol?L-1?s-1;
(2)t3~t4阶段与t4~t5阶段正逆反应速率都相等,而t3~t4阶段为使用催化剂,如t4~t5阶段改变的条件为降低反应温度,平衡移动发生移动,则正逆反应速率不相等,则t4~t5阶段应为减小压强;反应中A的浓度变化为0.15mol/L-0.06mol/L=0.09mol/L,C的浓度变化为0.11mol/L-0.05mol/L=0.06mol/L,反应中A与C的计量数之比为0.09:0.06=3:2,
则该反应中气体的化学计量数之和前后相等,则有:3A(g) B(g)+2C(g),
B(g)+2C(g),
根据方程式可知消耗0.09mol/L的A,则生成0.03mol/L的B,容器的体积为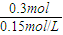 =2L,生成B的物质的量为0.03mol/L×2L=0.06mol,平衡时B的物质的量为0.05mol/L×2L=0.1mol,所以起始时B的物质的量为0.1mol-0.06mol=0.04mol,
=2L,生成B的物质的量为0.03mol/L×2L=0.06mol,平衡时B的物质的量为0.05mol/L×2L=0.1mol,所以起始时B的物质的量为0.1mol-0.06mol=0.04mol,
故答案为:减小压强;0.04mol;
(3)反应的方程式为3A(g) B(g)+2C(g),A的物质的量减少0.03mol,而此过程中容器与外界的热交换总量为akJ,则A的物质的量减少3mol,与外界的热交换总量为100akJ,由图象可知t5~t6阶段应为升高温度,A的物质的量减少,说明向正反应方向移动,则正反应吸热,该反应的热化学方程式为3A(g)
B(g)+2C(g),A的物质的量减少0.03mol,而此过程中容器与外界的热交换总量为akJ,则A的物质的量减少3mol,与外界的热交换总量为100akJ,由图象可知t5~t6阶段应为升高温度,A的物质的量减少,说明向正反应方向移动,则正反应吸热,该反应的热化学方程式为3A(g) B(g)+2C(g)△H=+100akJ?mol-1,
B(g)+2C(g)△H=+100akJ?mol-1,
故答案为:3A(g) B(g)+2C(g);△H=+100akJ?mol-1.
B(g)+2C(g);△H=+100akJ?mol-1.
点评:本题考查化学平衡移动图象题,题目难度较大,注意从乙图判断各阶段的影响因素,此为解答该题的关键,易错点为(2)中B的物质的量的计算.
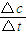 计算反应速率;
计算反应速率;(2)t4~t5阶段正逆反应速率减小且相等,如是降低温度,平衡移动发生移动,则正逆反应速率不相等;
根据C、A浓度的变化判断二者计量数关系,根据t4~t5阶段判断化学方程式,根据化学方程式计算;
(3)计算3molA反应的热量,结合方程式书写热化学方程式.
解答:解:(1)若t1=15s,生成物C在t~t1时间段的平均反应速率为:v=
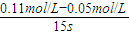 =0.004mol?L-1?s-1,故答案为:0.004mol?L-1?s-1;
=0.004mol?L-1?s-1,故答案为:0.004mol?L-1?s-1;(2)t3~t4阶段与t4~t5阶段正逆反应速率都相等,而t3~t4阶段为使用催化剂,如t4~t5阶段改变的条件为降低反应温度,平衡移动发生移动,则正逆反应速率不相等,则t4~t5阶段应为减小压强;反应中A的浓度变化为0.15mol/L-0.06mol/L=0.09mol/L,C的浓度变化为0.11mol/L-0.05mol/L=0.06mol/L,反应中A与C的计量数之比为0.09:0.06=3:2,
则该反应中气体的化学计量数之和前后相等,则有:3A(g)
 B(g)+2C(g),
B(g)+2C(g),根据方程式可知消耗0.09mol/L的A,则生成0.03mol/L的B,容器的体积为
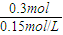 =2L,生成B的物质的量为0.03mol/L×2L=0.06mol,平衡时B的物质的量为0.05mol/L×2L=0.1mol,所以起始时B的物质的量为0.1mol-0.06mol=0.04mol,
=2L,生成B的物质的量为0.03mol/L×2L=0.06mol,平衡时B的物质的量为0.05mol/L×2L=0.1mol,所以起始时B的物质的量为0.1mol-0.06mol=0.04mol,故答案为:减小压强;0.04mol;
(3)反应的方程式为3A(g)
 B(g)+2C(g),A的物质的量减少0.03mol,而此过程中容器与外界的热交换总量为akJ,则A的物质的量减少3mol,与外界的热交换总量为100akJ,由图象可知t5~t6阶段应为升高温度,A的物质的量减少,说明向正反应方向移动,则正反应吸热,该反应的热化学方程式为3A(g)
B(g)+2C(g),A的物质的量减少0.03mol,而此过程中容器与外界的热交换总量为akJ,则A的物质的量减少3mol,与外界的热交换总量为100akJ,由图象可知t5~t6阶段应为升高温度,A的物质的量减少,说明向正反应方向移动,则正反应吸热,该反应的热化学方程式为3A(g) B(g)+2C(g)△H=+100akJ?mol-1,
B(g)+2C(g)△H=+100akJ?mol-1,故答案为:3A(g)
 B(g)+2C(g);△H=+100akJ?mol-1.
B(g)+2C(g);△H=+100akJ?mol-1.点评:本题考查化学平衡移动图象题,题目难度较大,注意从乙图判断各阶段的影响因素,此为解答该题的关键,易错点为(2)中B的物质的量的计算.

练习册系列答案
相关题目
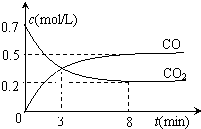 一定条件下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应:Fe(s)+CO2(g)?FeO(s)+CO(g)△H>0.反应过程中CO2气体和CO气体的浓度与时间的关系如图所示,下列说法不正确的是( )
一定条件下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应:Fe(s)+CO2(g)?FeO(s)+CO(g)△H>0.反应过程中CO2气体和CO气体的浓度与时间的关系如图所示,下列说法不正确的是( )A、该反应的平衡常数表达式为K=
| ||
B、升高温度后达新平衡时,
| ||
| C、3分钟时,CO和CO2的浓度相等,反应达到平衡状态 | ||
| D、8分钟内CO的平均反应速率v(CO)=0.0625 mol?L-1?min-1 |
 (2013?青岛一模)碳、氮和铝的单质及其化合物在工农业生产和生活中有重要的作用.
(2013?青岛一模)碳、氮和铝的单质及其化合物在工农业生产和生活中有重要的作用.