题目内容
下列实验中所选用的仪器合理的是
- A.用100mL量筒量取5.2mL的稀硫酸
- B.用500mL容量瓶配制500mL0.2mol/L的NaOH溶液
- C.用托盘天平称量11.75gNaCl晶体
- D.用分液漏斗进行固体和液体的分离
B
分析:A、从减小实验误差的角度去选择量筒的量程;
B、根据容量瓶的使用规则进行解答;
C、根据托盘天平的精确到的最小值来判断;
D、根据漏斗进行固体和液体的分离进行解答.
解答:A、量取5.2mL的稀硫酸应选用10mL量筒而不是100mL量筒,故A错误;
B、用500mL容量瓶只能配制500mL0.2mol/L的NaOH溶液,故B正确;
C、托盘天平能准确到0.1g,用托盘天平不能用托盘天平称量11.75gNaCl晶体,故C错误;
D、漏斗进行固体和液体的分离,而不是分液漏斗,故D错误.
故选:B.
点评:本题考查托盘天平、量筒、容量瓶的使用,都是实验中经常遇到的问题,需要同学们认真审题并好好掌握.
分析:A、从减小实验误差的角度去选择量筒的量程;
B、根据容量瓶的使用规则进行解答;
C、根据托盘天平的精确到的最小值来判断;
D、根据漏斗进行固体和液体的分离进行解答.
解答:A、量取5.2mL的稀硫酸应选用10mL量筒而不是100mL量筒,故A错误;
B、用500mL容量瓶只能配制500mL0.2mol/L的NaOH溶液,故B正确;
C、托盘天平能准确到0.1g,用托盘天平不能用托盘天平称量11.75gNaCl晶体,故C错误;
D、漏斗进行固体和液体的分离,而不是分液漏斗,故D错误.
故选:B.
点评:本题考查托盘天平、量筒、容量瓶的使用,都是实验中经常遇到的问题,需要同学们认真审题并好好掌握.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
Ⅰ.下图为常见仪器的部分结构(有的仪器被放大)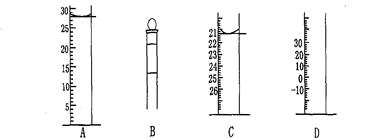
图A中液面所示溶液的体积为 mL,用上述四种仪器中的某种测量一液体的体积,平视时读数为n mL,仰视时读数为m mL,若m>n,则所使用的仪器是 (填字母标号)。
Ⅱ.某学生用标准0.25 mol·L—1 NaOH溶液滴定硫酸的实验操作如下:
| A.用酸式滴定管取稀H2SO4 25.00 mL,注入锥形瓶中,加入指示剂。 | |
| B.用待测定的溶液润洗酸式滴定管。 | C.用蒸馏水洗干净滴定管。 |
| D.取下碱式滴定管用标准的NaOH溶液润洗后,将标准液注入碱式滴定管刻度“0”以上2~3 cm处,再把碱式滴定管固定好,调节液面至刻度“0”或“0”刻度以下。 |
G.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度。
①滴定操作的正确顺序是(用序号填): 。
②该滴定操作中应选用的指示剂是: 。
③在G操作中如何确定终? 。
④碱式滴定管用蒸馏水润洗后,未用标准液润洗导致滴定结果(填“偏小”、“偏大”或“恰好合适”) ,原因是 。
⑤假设操作均正确,标准液消耗了22.18mL,计算待测硫酸溶液的物质的量浓度(计算结果精确到小数点后二位) mol·L—1
Ⅲ.已知常温时醋酸的电离常数为1.8×10-5,一水合氨的电离常数为1.8×10-5。在少量Mg(OH)2悬浊液中,滴加适量饱和NH4Cl溶液,固体溶解。对于固体的溶解。
甲同学认为在氢氧化镁悬浊液中存在下列平衡:
Mg(OH)2
 Mg2+ +2OH-
Mg2+ +2OH-加入NH4Cl溶液,由于NH4+水解产生H+中和了Mg(OH)2电离产生的OH-而使平衡右移导致Mg(OH)2 溶解。
而乙同学却认为NH4Cl电离产生的NH4+结合了OH-生成了弱电解质NH3·H2O,使c(OH-)减小,平衡右移而导致Mg(OH)2 溶解。设计方案评价甲乙两位同学的观点:
_____________________________________ ______________________________
_________________________________________________________________________
 仪器如图所示(装置可重复使用)。回答下列问题:
仪器如图所示(装置可重复使用)。回答下列问题: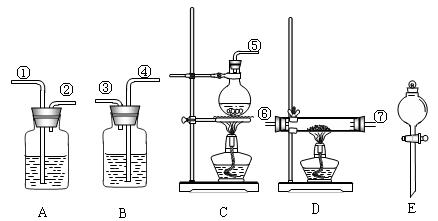
 Mg2+ +2OH-
Mg2+ +2OH-