题目内容
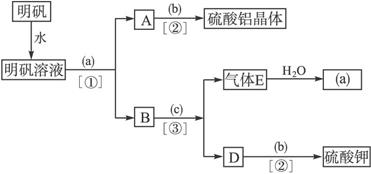
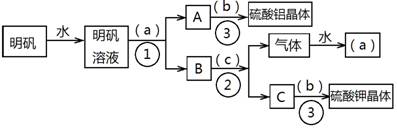
下图是用明矾〔KAl(SO4)2·12H2O〕为主要原料制取Al2(SO4)3和K2SO4的操作步骤流程图(图中略去了沉淀物的洗涤操作):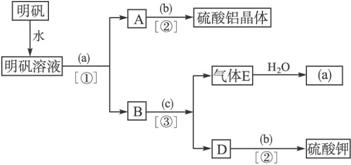
分析图中圆括号内应填入何种试剂,使用何种分离方法,并回答下列问题。
(1)试剂a是_____________,b是_____________,c是_____________,分离方法①是_____________,②是_____________,③是_____________。
(2)用离子反应方程式表示下列转化过程:
明矾溶液+a![]() A+B:_____________。B+C
A+B:_____________。B+C![]() E:_____________。
E:_____________。
(3)按上述操作不考虑损耗在理论上
解析:根据题目要求和操作步骤流程图,可以判断:分离Al元素应选用的试剂为氨水,即a为氨水(NH3·H2O),A为氢氧化铝沉淀,b为稀硫酸,与氢氧化铝沉淀反应生成硫酸铝;B为硫酸铵,c为氢氧化钾,气体E应为氨气。操作①是过滤,操作②是结晶,操作③是加热,使氨气挥发。若按上述操作不考虑损耗在理论上
答案:(1)NH3·H2O H2SO4 KOH 过滤 结晶 加热
(2)Al3++3NH3·H2O![]() Al(OH)3↓+3
Al(OH)3↓+3![]()
![]() +OH-
+OH-![]() NH3↑+H2O
NH3↑+H2O
(3)111 115

练习册系列答案
相关题目