题目内容
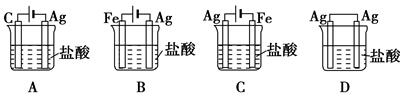
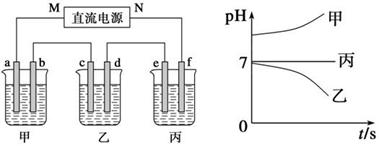
用两支惰性电极插入500mL AgNO3溶液中,通电电解。当电解液的pH从6.0变为3.0时(电解时阴极没有氢气放出,且电解液在前后体积变化可以忽略),阴极上析出的质量大约是( )
| A.27mg | B.54 mg | C.108 mg | D.216 mg |
B
根据题意可知氢离子浓度的变化量是(10-3-10-6)mol/L=10-3mol/L,所以反应中生成的氢离子的物质的量是0.5L×1010-3mol/L=5×10-4mol。惰性电极电解硝酸银的反应式为4AgNO3+2H2O 4HNO3+4Ag+O2↑,所以析出的银也是5×10-4mol,其质量是5×10-4mol×108g/mol=0.054g=54mg,答案选B。
4HNO3+4Ag+O2↑,所以析出的银也是5×10-4mol,其质量是5×10-4mol×108g/mol=0.054g=54mg,答案选B。
 4HNO3+4Ag+O2↑,所以析出的银也是5×10-4mol,其质量是5×10-4mol×108g/mol=0.054g=54mg,答案选B。
4HNO3+4Ag+O2↑,所以析出的银也是5×10-4mol,其质量是5×10-4mol×108g/mol=0.054g=54mg,答案选B。
练习册系列答案
相关题目