��Ŀ����
����Ŀ����ͼ��һ����ѧ���̵�ʾ��ͼ�� 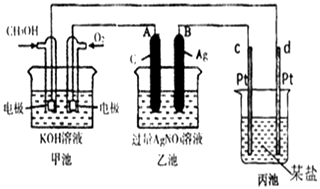
��1����ش�ͼ�м׳���װ�ã�����OH���������������������
��2��д��ͨ��CH3OH�ĵ缫��Ӧʽ��
��3�����ҳ����缫�����μ�������ɫʯ����Һ���������ĵ缫Ϊ�����A����B��������д���˵缫��Ӧ�ĵ缫��Ӧʽ ��
��4���ҳ��з�Ӧ�����ӷ���ʽΪ ��
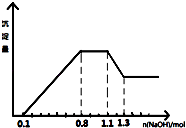
��5�����ҳ���B��Ag��������������2.70gʱ���ҳص�pH��������ʱ�ҳ�����Һ�����Ϊ250mL������ʱ����ij�缫����0.80gij����������е�ij����Һ������������ţ�
A��MgSO4 B��CuSO4 C��NaCl D��AgNO3 ��
���𰸡�
��1��ԭ��أ���
��2��CH3OH��6e��+8OH��=CO32��+6H2O
��3��A��4H2O��4e��=O2��4H+
��4��4Ag++2H2O ![]() 4Ag+O2��+4H+
4Ag+O2��+4H+
��5��1��BD
���������⣺��1��ȼ�ϵ���ǻ�ѧ��ת��Ϊ���ܵ�װ�ã�����ԭ��أ�ȼ�ϵ���У�Ͷ��ȼ�ϵĵ缫�Ǹ�����Ͷ���������ĵ缫��������ԭ��طŵ�ʱ���������Һ���������������ƶ�������Ͷ�ż״��ĵ缫�ƶ������Դ��ǣ�ԭ��أ�������2����ȼ�ϵ���У��״�ʧ���Ӻ����������ӷ�Ӧ����̼������Ӻ�ˮ���缫��ӦʽΪ��CH3OH��6e��+8OH��=CO32��+6H2O��
���Դ��ǣ�CH3OH��6e��+8OH��=CO32��+6H2O����3���ҳ�����ӵ�Դ���ڵ��أ�����ԭ���������A������������ԭ��ظ�����B�������������������Һʱ��A�缫��ˮ�õ������������������ӣ���Һ�����ԣ�������ɫʯ����Һ�ʺ�ɫ���缫��ӦʽΪ4H2O��4e��=O2��4H+ ��
���Դ��ǣ�A��4H2O��4e��=O2��4H+����4�������������Һʱ�������ӵõ�����������ˮʧ�������������������ӣ����ӷ���ʽΪ4Ag++2H2O ![]() 4Ag+O2��+4H+ ��
4Ag+O2��+4H+ ��
���Դ��ǣ�4Ag++2H2O ![]() 4Ag+O2��+4H+����5�����ҳ���B��Ag��������������2.70gʱ����������Ũ��Ϊxmol/L��
4Ag+O2��+4H+����5�����ҳ���B��Ag��������������2.70gʱ����������Ũ��Ϊxmol/L��
4Ag+ | + | 2H2O | = | 4Ag | + | O2�� | + | 4H+ |
432g | 4mol | |||||||
2.70g | 0.25xmol |
x=0.1������Һ��pH=1���������������������ڽ������˳����н���Ԫ�ش���HԪ�غ��ݴ��������ת�Ƶ��������֪��������������Ԫ����Ҫ�ĵ��ӵ��ڻ�С���ҳ���ת�Ƶ��������ݴ�ȷ�����еĽ���Ԫ�أ�����2.70gʱת�Ƶ�����0.025mol��
A������þ��þԪ�ش���HԪ��ǰ�����������ϲ������������ʣ��ʴ���
B���������ͭ��Һʱ������������0.8gͭ��Ҫת�Ƶ���0.025mol������ȷ��
C���Ȼ�������Ԫ�ش�����Ԫ��ǰ�����������ϲ������������ʣ��ʴ���
D�������������Һʱ������������0.80g����Ҫת�Ƶ���0.0074mol��0.025mol������ȷ��
��ѡBD��
���Դ��ǣ�1��BD��

����Ŀ��Ϊ̽��FeCl3��Һ�е�����ƽ������ӷ�Ӧ��ijС��ͬѧ����������ʵ��
��1������50mL 1.0mol��L-1 ��FeCl3 ��Һ������pHԼΪ0.7����c(H+)=0.2mol��L-1��
���û�ѧ�������FeCl3��Һ�����Ե�ԭ��__________________��
������ʵ�鷽���У���ʹFeCl3��ҺpH���ߵ���___________������ĸ��ţ���
a. ��ˮϡ�� b. ����FeCl3���� c. �μ�ŨKSCN��Һ d. ����NaHCO3����
��2��С��ͬѧ��������FeCl3��Һ̽����������п�۵ķ�Ӧ��ʵ��������������£�
���� | ���� |
��Ӧƿ�м���6.5 gп�ۣ�Ȼ�����50mL 1.0mol��L-1 ��FeCl3 ��Һ������ | ��Һ�¶�Ѹ���������Ժ���ֺ��ɫ������ͬʱ�����������ݣ���Ӧһ��ʱ����ã��ϲ���ҺΪdz��ɫ����Ӧƿ�ײ��к�ɫ���� |
�ռ����鷴Ӧ�����в��������� | �����ܿڿ������棬�б����� |
��֪��Zn��������Al���ƣ��ܷ�����Ӧ��Zn��2NaOH=Na2ZnO2��H2��
�ٽ��ʵ�������ƽ���ƶ�ԭ�����ͳ��ֺ��ɫ������ԭ��_________________________�� �������ӷ���ʽ���ͷ�Ӧ����ҺΪdz��ɫ��ԭ��______________________________��
�۷������ɫ���壬������ʵ��֤ʵ�����к��е���Ҫ���ʡ�
i. ��ɫ������Ա�����������
ii. ���ɫ�����м���������NaOH��Һ���������ݣ�
iii. ��ii��ʣ�����������ˮϴ�Ӻ���ϡ���ᣬ�����������ݣ�
iv. ��iii��Ӧ�����Һ�еμ�KSCN��Һ���ޱ仯��
a. ��ɫ������һ�����е�������______________��
b. С��ͬѧ��Ϊ����ʵ����ȷ����ɫ�������Ƿ���Fe3O4��������________________��