题目内容
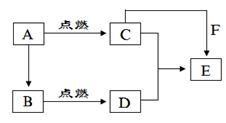
(12分)已知A是生产生活中用量最大的金属,B为淡黄色粉末。在常温下C为无色液体,E、G、H、I、J为气体,其中H为黄绿色,其它为无色。J能使湿润的红色石蕊试纸变蓝(图中部分产物已略去)。

请填写下列空白
(1)写出化学式:D ,K 。
(2)写出②的离子方程式 。
(3)反应④不属于下列何种反应类型 (填字母序号)。
A. 化合反应 B. 氧化还原反应 C. 离子反应 D. 置换反应
(4)若要确定③反应后所得溶液中含有M物质,所选试剂为 (填序号)。
A. KSCN溶液和氯水 B. 铁粉和KSCN
C. 浓氨水 D. 酸性高锰酸钾溶液
(5)将F加入到M的溶液里并露置在空气中,可以观察到整个过程的现象是:
。
(6)常温下,H与过量的J反应产生浓厚的白烟,另一生成物是空气的主要成分之一,请写出该反应的化学方程式 。

请填写下列空白
(1)写出化学式:D ,K 。
(2)写出②的离子方程式 。
(3)反应④不属于下列何种反应类型 (填字母序号)。
A. 化合反应 B. 氧化还原反应 C. 离子反应 D. 置换反应
(4)若要确定③反应后所得溶液中含有M物质,所选试剂为 (填序号)。
A. KSCN溶液和氯水 B. 铁粉和KSCN
C. 浓氨水 D. 酸性高锰酸钾溶液
(5)将F加入到M的溶液里并露置在空气中,可以观察到整个过程的现象是:
。
(6)常温下,H与过量的J反应产生浓厚的白烟,另一生成物是空气的主要成分之一,请写出该反应的化学方程式 。
(1)Fe3O4,NH4Cl(2分,各1分)
(2)2Na2O2+2H2O =4Na++4OH—+O2↑(2分)
(3)D(1分)(4)D(3分)
(5)产生白色沉淀,迅速变成灰绿色,最后变成红褐色(2分)
(6)8NH3+3Cl2=N2+6NH4Cl(2分)
(2)2Na2O2+2H2O =4Na++4OH—+O2↑(2分)
(3)D(1分)(4)D(3分)
(5)产生白色沉淀,迅速变成灰绿色,最后变成红褐色(2分)
(6)8NH3+3Cl2=N2+6NH4Cl(2分)
试题分析:由题中所给信息,A是金属铁,常温下C为无色液体只能是水,A能和水蒸气反应生成D(四氧化三铁)和E(氢气)。H为黄绿色,所以H是氯气,I是氯化氢。又有J能使湿润的红色石蕊试纸变蓝也是解本题的突破口,可得J为氨气,所以K为NH4Cl。B为淡黄色粉末,可能是单质硫、过氧化钠、溴化银等,依据转化关系可知B只能是过氧化钠,其和水反应生成G(氧气)和F(氢氧化钠),F(氢氧化钠)和K(NH4Cl)反应生成无色气体J(氨气)。
D(四氧化三铁)和I(氯化氢)的溶液反应生成N(氯化铁)和M(氯化亚铁),M(氯化亚铁)可以和H(氯气)反应生成N(氯化铁)。检验③反应后所得混合溶液中M(氯化亚铁)的存在,不能选A、B、D,因为溶液中存在显黄色的三价铁离子,所以只能用氨水检验。
点评:本题主要考查根据题给信息和实验现象正确判断物质类别,解答推断题要抓住几个重要的突破口,如物质的颜色、反应溶液的颜色等。

练习册系列答案
相关题目