题目内容
| 元素代号 | 相关信息 |
| A | A的单质能与冷水剧烈反应,得到强碱性溶液 |
| B | B的原子最外层电子数是其内层电子数的三倍 |
| C | 在第3周期元素中,C的简单离子半径最小 |
| D | A、B、D组成的36电子的化合物X是家用消毒剂的主要成分 |
| E | 所有有机物中都含有E元素 |

(2)X的化学式为
(3)A、B、C三种元素形成的简单离子的半径由大到小的顺序为
(4)A在真空压下能与由元素D、E组成的化合物ED4反应生成两种固体物质,其中一种是自然界中硬度最大的物质,此反应在科学上有“稻草变黄金”的美称.写出该反应的化学方程式
| ||
| ||
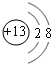
(1)E为碳元素,原子有2个电子层,最外层电子数为4,处于周期表中第二周期第ⅣA族;C为铝元素,铝离子核外电子数为10,有2个电子层,最外层电子数为8,离子结构示意图为
 ,故答案为:第二周期第ⅣA族;
,故答案为:第二周期第ⅣA族; ;
;(2)有上述分析可知,X为NaClO,故答案为:NaClO;
(3)A、B、C三种元素形成的简单离子分别为Na+、O2-、Al3+,离子的电子层排布相同,核电荷数越大,离子半径越小,所以离子半径由大到小的顺序为O2->Na+>Al3+,
故答案为:O2->Na+>Al3+;
(4)Na在真空压下能与化合物CCl4反应生成两种固体物质,其中一种是自然界中硬度最大的物质,该物质为金刚石,另外物质为氯化钠,反应方程式为4Na+CCl4
| ||
故答案为:4Na+CCl4
| ||

(8分)阅读下表中短周期主族元素的相关信息。
|
元素代号 |
8相关信息 |
|
A |
A的单质能与冷水剧烈反应,得到强碱性溶液 |
|
B |
B的原子最外层电子数是其内层电子数的三倍 |
|
C |
在第三周期元素中,C的离子半径简单最小 |
|
D |
A、B、D组成的36电子的化合物X是家用消毒剂的主要成分 |
|
E |
所有有机物中都含有E元素 |
请回答:
(1)写出E在元素周期表中的位置:_________;C的简单离子的结构示意图:__________;
(2)写出A2B2晶体中存在的化学键有:_______________________;
(3)A在真空高压下能与由D、E组成的分子呈正四面体结构的化合物Y反应生成2种固体物质,其中一种是自然界中硬度最大的物质,此反应在科学上有“稻草变黄金”的美称。请写出该反应的化学方程式:_________________________________________________;
(4)常温下,0.1 mol·L-1X溶液的pH 7(填“>”、“=”或“<”)。简述X可以做家用消毒剂的理由:________________________________________________________。
(8分)阅读下表中短周期主族元素的相关信息。
|
元素代号 |
8相关信息 |
|
A |
A的单质能与冷水剧烈反应,得到强碱性溶液 |
|
B |
B的原子最外层电子数是其内层电子数的三倍 |
|
C |
在第三周期元素中,C的离子半径简单最小 |
|
D |
A、B、D组成的36电子的化合物X是家用消毒剂的主要成分 |
|
E |
所有有机物中都含有E元素 |
请回答:
(1)写出E在元素周期表中的位置:_________;C的简单离子的结构示意图:__________;
(2)写出A2B2晶体中存在的化学键有:_______________________;
(3)A在真空高压下能与由D、E组成的分子呈正四面体结构的化合物Y反应生成2种固体物质,其中一种是自然界中硬度最大的物质,此反应在科学上有“稻草变黄金”的美称。请写出该反应的化学方程式:_________________________________________________;
(4)常温下,0.1 mol·L-1X溶液的pH 7(填“>”、“=”或“<”)。简述X可以做家用消毒剂的理由:________________________________________________________。
阅读下表中短周期主族元素的相关信息。
|
元素代号 |
相关信息 |
|
A |
A的单质能与冷水剧烈反应,得到强碱性溶液 |
|
B |
B的原子最外层电子数是其内层电子数的三倍 |
|
C |
在第3周期元素中,C的简单离子半径最小 |
|
D |
A、B、D组成的36电子的化合物X是家用消毒剂的主要成分 |
|
E |
所有有机物中都含有E元素 |
请回答:(1)、在一定条件下,B2与C的单质在海水中可形成原电池,为新型海水航标灯提供能源。写出该原电池正极的电极反应式 。
(2)、用惰性电极电解化合物AD的水溶液,该反应的化学方程式为:
其中,阴极产物是
(3)、常温下,0.1 mol·L-1X溶液的pH 7(填“>”、“=”或“<”),原因是 (用离子方程式说明)。
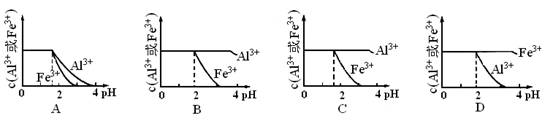
(4)、已知Ksp[Al(OH)3]=1.3×10-33,Ksp[Fe(OH)3]=4.0×10-38。
现向pH=0,浓度均为0.04mol·L-1的Al3+、Fe3+溶液中加入A的最高价氧化物对应水化物的溶液,以调节pH(设溶液体积不变),该过程中Al3+、Fe3+的浓度与pH关系正确的是
(填字母代号)。
(8分)阅读下表中短周期主族元素的相关信息。
|
元素代号 |
8相关信息 |
|
A |
A的单质能与冷水剧烈反应,得到强碱性溶液 |
|
B |
B的原子最外层电子数是其内层电子数的三倍 |
|
C |
在第三周期元素中,C的离子半径简单最小 |
|
D |
A、B、D组成的36电子的化合物X是家用消毒剂的主要成分 |
|
E |
所有有机物中都含有E元素 |
请回答:
(1)写出E在元素周期表中的位置:_________;C的简单离子的结构示意图:__________;
(2)写出A2B2晶体中存在的化学键有:_______________________;
(3)A在真空高压下能与由D、E组成的分子呈正四面体结构的化合物Y反应生成2种固体物质,其中一种是自然界中硬度最大的物质,此反应在科学上有“稻草变黄金”的美称。请写出该反应的化学方程式:_________________________________________________;
(4)常温下,0.1 mol·L-1X溶液的pH 7(填“>”、“=”或“<”)。简述X可以做家用消毒剂的理由:________________________________________________________。