题目内容
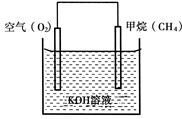
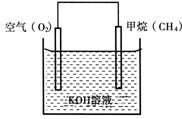
下图为甲烷燃料电池原理示意图,按照此图的提示,下列叙述不正确的是
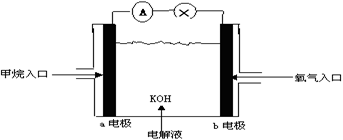
- A.a电极是负极
- B.b电极的电极反应为:4OH- -4e- →2H2O +O2 ↑
- C.甲烷燃料电池是一种具有应用前景的绿色电源
- D.甲烷燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置
该装置为燃料电池装置,在燃料电池中,通入燃料的一极为负极,通入空气(或氧气)的一极为正极;所以
A正确,甲烷为燃料,所以通入负极;B错,b电极(正极)的电极反应为:O2+4e- +2H2O→4OH-;
C正确,燃料电池是一种具有应用前景的绿色电源,不污染环境或对环境污染小;
D正确,甲烷燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置

 阅读快车系列答案
阅读快车系列答案(13 分)
(1)CuSO4溶液是中学化学及工农业生产中常见的一种试剂。某同学利用CuSO4溶液,进行以下实验探究。
① 图一是根据反应Zn + CuSO4 =" Cu" + ZnSO4设计成的锌铜原电池。电解质甲溶液是 (填“ZnSO4”或“CuSO4”)溶液;Cu极的电极反应式是 。
②图二中,Ⅰ是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,该同学想在Ⅱ中实现铁上镀铜,则b处通入的是 (填“CH4”或“O2”),a处电极上发生的电极反应式是 。
(2)将蓝矾(CuSO4·5H2O)、生石灰和水按一定比例混合,即可得到波尔多液(杀菌剂),其有效成分为难溶的碱式硫酸铜[xCuSO4 ·yCu(OH)2]。为测定某碱式硫酸铜的组成进行了如下实验:取等质量的碱式硫酸铜样品两份,一份滴加稀盐酸至恰好完全溶解,另一份高温灼烧后只得到CuO固体。所得数据显示n(HCl)︰n(CuO)=3︰2,则该碱式硫酸铜的化学式中x︰y= 。
(3)E是非金属性最强的元素,M是E的气态氢化物,在固定体积的密闭容器中,气体M存在如下关系:
xM(g) Mx(g),反应物和生成物的物质的量随时间的变化关系如下图。下 列说法正确的是
Mx(g),反应物和生成物的物质的量随时间的变化关系如下图。下 列说法正确的是 
A.该反应的化学方程式是2HF (HF)2 (HF)2 |
| B.平衡时混合气体的平均摩尔质量是33.3 |
C.t1时刻,保持温度不变,再充入1molM,重新达到平衡时, 将增大 将增大 |
| D.M的沸点比同主族下一周期元素的气态氢化物沸点低 |
(13 分)
(1)CuSO4溶液是中学化学及工农业生产中常见的一种试剂。某同学利用CuSO4溶液,进行以下实验探究。
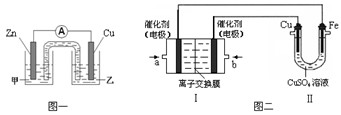
① 图一是根据反应Zn + CuSO4 = Cu + ZnSO4 设计成的锌铜原电池。电解质甲溶液是 (填“ZnSO4”或“CuSO4”)溶液;Cu极的电极反应式是 。
②图二中,Ⅰ是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,该同学想在Ⅱ中实现铁上镀铜,则b处通入的是 (填“CH4”或“O2”),a处电极上发生的电极反应式是 。
(2)将蓝矾(CuSO4·5H2O)、生石灰和水按一定比例混合,即可得到波尔多液(杀菌剂),其 有效成分为难溶的碱式硫酸铜[xCuSO4 ·yCu(OH)2]。为测定某碱式硫酸铜的组成进行了如下实验:取等质量的碱式硫酸铜样品两份,一份滴加稀盐酸至恰好完全溶解,另一份高温灼烧后只得到CuO固体。所得数据显示n(HCl)︰n(CuO)=3︰2,则该碱式硫酸铜的化学式中x︰y= 。
(3)E是非金属性最强的元素,M是E的气态氢化物,在固定体积的密闭容器中,气体M存在如下关系:
xM(g) Mx
(g),反应物和生成物的物质的量随时间的变化关系如下图。下 列说法正确的是
Mx
(g),反应物和生成物的物质的量随时间的变化关系如下图。下 列说法正确的是
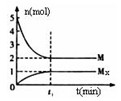
B.平衡时混合气体的平均摩尔质量是33.3
C.t1时刻,保持温度不变,再充入1molM,重新达到平衡时, 将增大
将增大
D.M的沸点比同主族下一周期元素的气态氢化物沸点低
 将增大
将增大