题目内容
【题目】在探究新制饱和氯水成分的实验中,下列根据实验现象得出的结论不正确的是
A.氯水的颜色呈浅黄绿色,说明氯水中含有Cl2
B.向氯水中加入NaHCO3粉末,有气泡产生,说明氯水中含有H+
C.向FeCl2溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中含有HClO
D.向氯水中滴加硝酸酸化的AgNO3溶液,产生白色沉淀,说明氯水中含有Cl-
【答案】C
【解析】
氯气溶于水,部分发生反应:Cl2+H2O![]() H++Cl-+HClO ,所以在氯水中含有Cl2、HClO、H2O、H+、Cl-、ClO-、OH-多种微粒。
H++Cl-+HClO ,所以在氯水中含有Cl2、HClO、H2O、H+、Cl-、ClO-、OH-多种微粒。
A.氯水的颜色呈浅黄绿色,就是由于氯水中含有Cl2,A正确;
B.向氯水中加入NaHCO3粉末,有气泡产生,是由于发生反应:HCO3-+OH-=H2O+CO32-,说明氯水中含有H+,B正确;
C.向FeCl2溶液中滴加氯水,溶液颜色变成棕黄色,是因为HClO、Cl2都有强氧化性,会把Fe2+氧化为Fe3+,不能说明氯水中是否含有HClO,C错误;
D.向氯水中滴加硝酸酸化的AgNO3溶液,发生反应Cl-+Ag+=AgCl↓,产生白色沉淀,说明氯水中含有Cl-,D正确;
故选C。

 名校课堂系列答案
名校课堂系列答案【题目】决定物质性质的重要因素是物质结构。请回答下列问题:
(1)已知元素M是组成物质Ca5(PO4)3F的一种元素。元素M的气态原子逐个失去第1个至第5个电子所需能量(即电离能,用符号I1至I表示)如表所示:
I1 | I2 | I3 | I4 | I5 | |
电离能(kJ/mol) | 589.8 | 1145.4 | 4912.4 | 6491 | 8153 |
元素M化合态常见化合价是___________价,其基态原子电子排布式为___________。
(2)往硫酸铜溶液中加入过量氨水,可形成[Cu(NH3)4]SO4,溶液,该溶液可用于溶解纤维素。
①[Cu(NH3)4]SO4中阴离子的立体构型是___________。
②除硫元素外,[Cu(NH3)4]SO4中所含元素的电负性由小到大的顺序为___________。
③NF3与NH3的空间构型相同,中心原子的轨道杂化类型均为___________。但NF3不易与Cu2+形成化学键,其原因是___________。
(3)一种Hg-Ba-Cu-O高温超导材料的晶胞(长方体)如图所示。
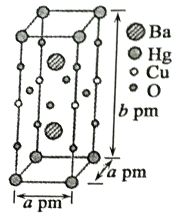
①该物质的化学式为___________。
②已知该晶胞中两个Ba2+的间距为cpm。则距离Ba2+最近的Hg+数目为___________个,二者的最短距离为___________pm。(列出计算式即可,下同)
③设该物质的摩尔质量为M,阿伏加德罗常数的值为NA,则该晶体的密度为___________g·cm-3。