题目内容
(10分)在容积为2 L的密闭容器中充入1 mol A和2 mol B,按2A(g)+B(g) 3C(g)进行反应,经4 min后,测得C的物质的量为0.6 mol,试计算分别用A、B、C三种不同物质表示的该反应的反应速率。
3C(g)进行反应,经4 min后,测得C的物质的量为0.6 mol,试计算分别用A、B、C三种不同物质表示的该反应的反应速率。
 3C(g)进行反应,经4 min后,测得C的物质的量为0.6 mol,试计算分别用A、B、C三种不同物质表示的该反应的反应速率。
3C(g)进行反应,经4 min后,测得C的物质的量为0.6 mol,试计算分别用A、B、C三种不同物质表示的该反应的反应速率。v(A)="0.05" mol·L-1·min-1,v(B)="0.025" mol·L-1·min-1,v(C)="0.075" mol·L-1·min-1
已知经4 min的时间n(C)变化0.6 mol,c(C)变化0.3 mol·L-1,可用v=Δc/Δt法求v(C)。又可用v(A)∶v(B)∶v(C)=2∶1∶3法求v(A)、v(B)。
经4 min后,生成物C的物质的量浓度变化值为
Δc(C)=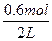 ="0.3" mol·L-1
="0.3" mol·L-1
v(C)=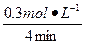 ="0.075" mol·L-1·min-1
="0.075" mol·L-1·min-1
v(A)∶v(B)∶v(C)=2∶1∶3
v(A)=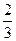 v(C)=
v(C)=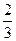 ×0.075 mol·L-1·min-1="0.05" mol·L-1·min-1
×0.075 mol·L-1·min-1="0.05" mol·L-1·min-1
v(B)=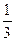 v(C)=
v(C)= 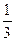 ×0.075 mol·L-1·min-1="0.025" mol·L-1·min-1
×0.075 mol·L-1·min-1="0.025" mol·L-1·min-1
经4 min后,生成物C的物质的量浓度变化值为
Δc(C)=
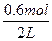 ="0.3" mol·L-1
="0.3" mol·L-1v(C)=
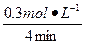 ="0.075" mol·L-1·min-1
="0.075" mol·L-1·min-1v(A)∶v(B)∶v(C)=2∶1∶3
v(A)=
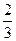 v(C)=
v(C)=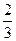 ×0.075 mol·L-1·min-1="0.05" mol·L-1·min-1
×0.075 mol·L-1·min-1="0.05" mol·L-1·min-1v(B)=
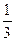 v(C)=
v(C)= 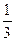 ×0.075 mol·L-1·min-1="0.025" mol·L-1·min-1
×0.075 mol·L-1·min-1="0.025" mol·L-1·min-1
练习册系列答案
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目
 2HI(g)(正反应吸热)
2HI(g)(正反应吸热) 2SO3(g);△H<0,应选择的适宜条件是( )
2SO3(g);△H<0,应选择的适宜条件是( ) 2AB3这一可逆反应,在一定时间内,以下为在不同条件下的反应速率,其中速率最大的是( )
2AB3这一可逆反应,在一定时间内,以下为在不同条件下的反应速率,其中速率最大的是( ) 2CO(g)反应中,可使反应速率增大的措施是( )
2CO(g)反应中,可使反应速率增大的措施是( )