题目内容
用惰性电极电解NaCl与NaHCO3的混合溶液,假设电解过程中产生的气体全部逸出,测得溶液pH变化如图所示.
(1)在0→t1时间内,两个电极上的电极反应式为:阳极______;阴极______.
(2)0→t1时间内,溶液pH升高比较缓慢的原因是(用离子方程式回答)______.
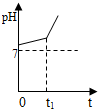
(1)在0→t1时间内,两个电极上的电极反应式为:阳极______;阴极______.
(2)0→t1时间内,溶液pH升高比较缓慢的原因是(用离子方程式回答)______.
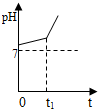
(1)在0→t1时间内,相当于电解氯化钠溶液,阳极上氯离子放电,电极反应式为2Cl--2e-═Cl2↑,阴极上氢离子放电,电极反应式为:2H++2e-═H2↑,
故答案为:2Cl--2e-=Cl2↑;2H++2e-=H2↑;
(2)用惰性电极电解氯化钠溶液时,阳极上析出氯气,阴极上析出氢气,同时溶液中还有氢氧化钠生成,氢氧化钠和碳酸氢钠反应生成碳酸钠,离子反应方程式为OH-+HCO3-═H2O+CO32-,所以溶液pH升高比较缓慢,故答案为:HCO3-+OH-=CO32-+H2O.
故答案为:2Cl--2e-=Cl2↑;2H++2e-=H2↑;
(2)用惰性电极电解氯化钠溶液时,阳极上析出氯气,阴极上析出氢气,同时溶液中还有氢氧化钠生成,氢氧化钠和碳酸氢钠反应生成碳酸钠,离子反应方程式为OH-+HCO3-═H2O+CO32-,所以溶液pH升高比较缓慢,故答案为:HCO3-+OH-=CO32-+H2O.

练习册系列答案
相关题目