��Ŀ����
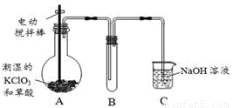
| A������ʵ��֤�������ԣ�ClO-��I2��SO42- |
| B������ʵ����еİ�ɫ������BaSO4��һ��������BaSO3 |
| C��ʵ���������������������Ժ����� |
| D��ʵ���֤��SO32-�������������л�ԭ�� |
���еķ�Ӧ����ʽNa2SO3+I2+H2O=Na2SO4+2HI��I2 �������Դ���SO4 2-�������ԣ�
����������ǿ��Ϊ��ClO-��I2��SO42-����A��ȷ��
B�����еμӹ�����Na2SO3��Һ��������Һ����Na2SO3��Na2SO4��Na2SO3��Na2SO4��BaCl2��Ӧ�����ɰ�ɫ��������B����
C�������еķ�Ӧ����ʽNaClO+2KI+H2SO4=I2+NaCl+K2SO4+H2O��H2SO4��Ӧǰ���Ԫ�صĻ��ϼ۶�û�仯��������������������ԣ���C����
D�����еķ�Ӧ����ʽNa2SO3+I2+H2O=Na2SO4+2HI��Na2SO3ʧ��������ԭ�������л�ԭ�ԣ���D����
��ѡA��

 ��У����ϵ�д�
��У����ϵ�д���15�֣��Ȼ����dz�����ˮ����������ˮ�Ȼ������۵�Ϊ555K���е�Ϊ588K����ҵ�Ʊ��Ȼ�����һ�ֹ������£�
�ش���������
��1��ȡ0.5mL�Ȼ�����Һ����50mL��ˮ�У������Ƭ�̵ú��ɫ��Һ�壬�ù��̿������ӷ���ʽ��ʾΪ ��
��2����֪FeCl3��6H2O��ˮ�е��ܽ�����£�
| �¶�/�� | 0 | 10 | 20 | 30 | 50 | 80 | 100 |
| �ܽ�ȣ�g/100gH2O�� | 74.4 | 81.9 | 91.8 | 106.8 | 315.1 | 525.8 | 535.7 |
��FeCl3��Һ�л��FeCl3��6H2O�ķ����� ��
��3�����������¶ȳ���673K��������Է�������Ϊ325�����ʣ������ʵĻ�ѧʽΪ ��
��4������ʱ��FeCl3��Һ�еμ�NaOH��Һ������Һ��c(Fe3+)��1.0��10-5 mol��L-1ʱ������Fe3+������ȫ����Fe3+������ȫ��pH����Ϊ ����֪Ksp��Fe(OH)3��=1.0��10-38����
��5�����ռ�X�� �������������ռ�X�������� ��
��6���ⶨ��Ʒ��FeCl3�����������ķ����ǣ�
a����ȡmg��ˮ�Ȼ�����Ʒ������ϡ���ᣬ��ת�Ƶ�100mL����ƿ��������ˮ����
b��ȡ��10mL������Һ����ƿ�У������Թ�����KI��Һ��ַ�Ӧ
c���Ե�����ָʾ������b mol��L-1Na2S2O3��Һ�ζ���I2+2 Na2S2O3=Na2S4O6+2NaI��������ȥVmL������Ʒ���Ȼ�������������Ϊ ��
�����������취�ⶨ����Ʒ��FeCl3����������ƫ�ͣ��ⶨ�����в��������ɺ��ԣ�����ԭ������� ��
��15�֣��Ȼ����dz�����ˮ����������ˮ�Ȼ������۵�Ϊ555K���е�Ϊ588K����ҵ�Ʊ��Ȼ�����һ�ֹ������£�
�ش���������
��1��ȡ0.5mL�Ȼ�����Һ����50mL��ˮ�У������Ƭ�̵ú��ɫ��Һ�壬�ù��̿������ӷ���ʽ��ʾΪ ��
��2����֪FeCl3��6H2O��ˮ�е��ܽ�����£�
| �¶�/�� | 0 | 10 | 20 | 30 | 50 | 80 | 100 |
| �ܽ�ȣ�g/100gH2O�� | 74.4 | 81.9 | 91.8 | 106.8 | 315.1 | 525.8 | 535.7 |
��3�����������¶ȳ���673K��������Է�������Ϊ325�����ʣ������ʵĻ�ѧʽΪ ��
��4������ʱ��FeCl3��Һ�еμ�NaOH��Һ������Һ��c(Fe3+)��1.0��10-5 mol��L-1ʱ������Fe3+������ȫ����Fe3+������ȫ��pH����Ϊ ����֪Ksp��Fe(OH)3��=1.0��10-38����
��5�����ռ�X�� �������������ռ�X�������� ��
��6���ⶨ��Ʒ��FeCl3�����������ķ����ǣ�
a����ȡmg��ˮ�Ȼ�����Ʒ������ϡ���ᣬ��ת�Ƶ�100mL����ƿ��������ˮ����
b��ȡ��10mL������Һ����ƿ�У������Թ�����KI��Һ��ַ�Ӧ
c���Ե�����ָʾ������b mol��L-1Na2S2O3��Һ�ζ���I2+2 Na2S2O3= Na2S4O6+2NaI��������ȥVmL������Ʒ���Ȼ�������������Ϊ ��
�����������취�ⶨ����Ʒ��FeCl3����������ƫ�ͣ��ⶨ�����в��������ɺ��ԣ�����ԭ������� ��
��15�֣��Ȼ����dz�����ˮ����������ˮ�Ȼ������۵�Ϊ555K���е�Ϊ588K����ҵ�Ʊ��Ȼ�����һ�ֹ������£�
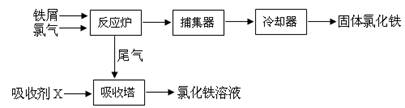
�ش���������
��1��ȡ0.5mL�Ȼ�����Һ����50mL��ˮ�У������Ƭ�̵ú��ɫ��Һ�壬�ù��̿������ӷ���ʽ��ʾΪ ��
��2����֪FeCl3��6H2O��ˮ�е��ܽ�����£�
|
�¶�/�� |
0 |
10 |
20 |
30 |
50 |
80 |
100 |
|
�ܽ�ȣ�g/100gH2O�� |
74.4 |
81.9 |
91.8 |
106.8 |
315.1 |
525.8 |
535.7 |
��FeCl3��Һ�л��FeCl3��6H2O�ķ����� ��
��3�����������¶ȳ���673K��������Է�������Ϊ325�����ʣ������ʵĻ�ѧʽΪ ��
��4������ʱ��FeCl3��Һ�еμ�NaOH��Һ������Һ��c(Fe3+)��1.0��10-5 mol��L-1ʱ������Fe3+������ȫ����Fe3+������ȫ��pH����Ϊ ����֪Ksp��Fe(OH)3��=1.0��10-38����
��5�����ռ�X�� �������������ռ�X�������� ��
��6���ⶨ��Ʒ��FeCl3�����������ķ����ǣ�
a����ȡmg��ˮ�Ȼ�����Ʒ������ϡ���ᣬ��ת�Ƶ�100mL����ƿ��������ˮ����
b��ȡ��10mL������Һ����ƿ�У������Թ�����KI��Һ��ַ�Ӧ
c���Ե�����ָʾ������b mol��L-1Na2S2O3��Һ�ζ���I2+2 Na2S2O3= Na2S4O6+2NaI��������ȥVmL������Ʒ���Ȼ�������������Ϊ ��
�����������취�ⶨ����Ʒ��FeCl3����������ƫ�ͣ��ⶨ�����в��������ɺ��ԣ�����ԭ������� ��