题目内容
金属冶炼和处理常涉及氧化还原反应。
(1)由下列物质冶炼相应金属时采用电解法的是 ,
a.Fe2O3 b.NaCl c.Cu2S d.Al2O3
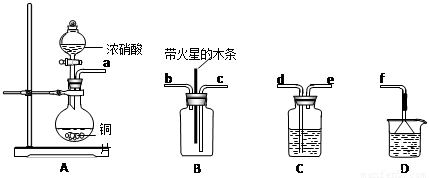
(2)辉铜矿(Cu2S)可发生反应2Cu2S+2H2SO4+5O2==4CuSO4+2H2O,该反应的还原剂是 ,当1mol O2发生反应时,还原剂所失电子的物质的量为 mol。向CuSO4溶液中加入镁条时有气体生成,该气体是 。
(3)下图为电解精炼银的示意图, (填“a”或“b”)极为含有杂质的粗银,若b极 有少量红棕色气体产生,则生成该气体的电极反应式为 ,

(4)为处理银器表面的黑斑(Ag2S),将银器置于铝制容器里的食盐水中并与铝接触,Ag2S转化为Ag,食盐水的作用为 。
(1)bd;
(2)Cu2S;4;H2;
(3)a;2H++NO3-+e-→NO2+H2O;
(4)做电解质溶液(或导电)。
【解析】
(1)金属的冶炼时,金属活动性顺序表中铝及其前面的金属一般采用电解法,故选bd;分析题给方程式:2Cu2S+2H2SO4+5O2==4CuSO4+2H2O,Cu元素和S元素的化合价均升高,O元素的化合价降低,故还原剂是Cu2S;当1mol O2发生反应时,氧化剂氧气得到4mol电子,则同时还原剂所失电子也为4mol;CuSO4溶液由于Cu2+水解呈酸性,故中加入镁条放出氢气;
(3)分析电解精炼银的装置,其中粗银应做阳极,故连接电源正极,是a极;b极是阴极,若生成红棕色的NO2气体,则是硝酸根放电:2H++NO3-+e-→NO2+H2O;
(4)处理银器时,食盐水的作用是做电解质溶液(或导电)。
【考点定位】此题考查了金属的冶炼、氧化还原反应、电解精炼和原电池知识。

 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南师范大学出版社系列答案
同步练习西南师范大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案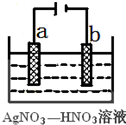 金属冶炼和处理常涉及氧化还原反应.
金属冶炼和处理常涉及氧化还原反应.