��Ŀ����
 �����������Ǵ�����Ⱦ����Ҫ���أ�
�����������Ǵ�����Ⱦ����Ҫ���أ���1�������ŷŵ�β���к�NO������NO�ķ�Ӧ�Ļ�ѧ����ʽΪ
��2����ȡ��ԭ������̿�ۿɽ��������ﻹԭ��
��֪��N2��g��+O2��g���T2NO��g����H=+180.6kJ?mol-1
C��s��+O2��g���TCO2��g����H=-393.5kJ?mol-1
��Ӧ C��s��+2NO��g���TCO2��g��+N2��g����H=
��3����NO2�������N2Ҫ�ҵ��ʺϵ�����G���ʵ��ķ�Ӧ������GӦΪ
NO2+G
| ���� |
���л������У�����������Ӧʽ�е�G��
a��NH3 b��CO2 c��SO2 d��CH3CH2OH
��4������ˮ����������Ⱦ�ķ����ǣ�
�ٴ����������У���H2��NO3-��ԭΪN2��һ��ʱ�����Һ�ļ���������ǿ����Ӧ�����ӷ���ʽΪ��
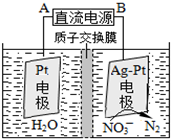
�������������£��绯ѧ����NO3-��ԭ����ͼ����Դ����Ϊ��
��������1�������������������������ת��Ϊһ��������
��2�����ݸ�˹���������㻯ѧ��Ӧ���ʱ䣻
��3������������ԭ��Ӧ���������ͻ�ԭ�����ص��ϳ������������ͻ�ԭ�����ش�
��4���ٸ�����Ϣ����H2��NO3-��ԭΪN2��һ��ʱ�����Һ�ļ���������ǿ�����������������ӣ��ݴ���д����ʽ��
���ڵ��ص������Ϸ����õ��ӵĻ�ԭ��Ӧ���ݴ���д�缫��Ӧ��
��2�����ݸ�˹���������㻯ѧ��Ӧ���ʱ䣻
��3������������ԭ��Ӧ���������ͻ�ԭ�����ص��ϳ������������ͻ�ԭ�����ش�
��4���ٸ�����Ϣ����H2��NO3-��ԭΪN2��һ��ʱ�����Һ�ļ���������ǿ�����������������ӣ��ݴ���д����ʽ��
���ڵ��ص������Ϸ����õ��ӵĻ�ԭ��Ӧ���ݴ���д�缫��Ӧ��
����⣺��1�������������������������ת��Ϊһ����������ӦΪ��N2+O2
2NO���ʴ�Ϊ��N2+O2
2NO��
��2����֪����N2��g��+O2��g���T2NO��g����H=+180.6kJ?mol-1
��C��s��+O2��g���TCO2��g����H=-393.5kJ?mol-1
��Ӧ C��s��+2NO��g���TCO2��g��+N2��g�������Ǣ�-�ٵõ������Ը÷�Ӧ�ġ�H=-393.5kJ?mol-1-180.6kJ?mol-1=-574.1kJ?mol-1��
�ʴ�Ϊ��C��s��+2NO��g���TCO2��g��+N2��g����H=-574.1kJ?mol-1��
��3����NO2�������N2�У���Ԫ�صĻ��ϼ۽����ˣ���������������������Ҫ���뻹ԭ�����������������ʣ�a��NH3 b��CO2 c��SO2 d��CH3CH2OH�У��ܱ����������������л�ԭ�Ե��������Ҵ���NH3���ʴ�Ϊ����ԭ����ad��
��4���ٸ�����Ϣ����H2��NO3-��ԭΪN2��һ��ʱ�����Һ�ļ���������ǿ�����������������ӣ������ķ�ӦΪ��2NO3-+5H2
N2+2OH-+4H2O��
�ʴ�Ϊ��2NO3-+5H2
N2+2OH-+4H2O��
�ڸ���װ��ͼʾ���Կ������Ҷ˵缫�Ϸ����õ��ӵĻ�ԭ��Ӧ����Ϊ��������ӦʽΪ��2NO3-+12 H++10e-=N2��+6H2O������B�Ǹ�����A��������
�ʴ�Ϊ��A��2NO3-+12 H++10e-=N2��+6H2O��
| ||
| ||
��2����֪����N2��g��+O2��g���T2NO��g����H=+180.6kJ?mol-1
��C��s��+O2��g���TCO2��g����H=-393.5kJ?mol-1
��Ӧ C��s��+2NO��g���TCO2��g��+N2��g�������Ǣ�-�ٵõ������Ը÷�Ӧ�ġ�H=-393.5kJ?mol-1-180.6kJ?mol-1=-574.1kJ?mol-1��
�ʴ�Ϊ��C��s��+2NO��g���TCO2��g��+N2��g����H=-574.1kJ?mol-1��
��3����NO2�������N2�У���Ԫ�صĻ��ϼ۽����ˣ���������������������Ҫ���뻹ԭ�����������������ʣ�a��NH3 b��CO2 c��SO2 d��CH3CH2OH�У��ܱ����������������л�ԭ�Ե��������Ҵ���NH3���ʴ�Ϊ����ԭ����ad��
��4���ٸ�����Ϣ����H2��NO3-��ԭΪN2��һ��ʱ�����Һ�ļ���������ǿ�����������������ӣ������ķ�ӦΪ��2NO3-+5H2
| ||
�ʴ�Ϊ��2NO3-+5H2
| ||
�ڸ���װ��ͼʾ���Կ������Ҷ˵缫�Ϸ����õ��ӵĻ�ԭ��Ӧ����Ϊ��������ӦʽΪ��2NO3-+12 H++10e-=N2��+6H2O������B�Ǹ�����A��������
�ʴ�Ϊ��A��2NO3-+12 H++10e-=N2��+6H2O��
���������⿼��ѧ���绯ѧ���Ȼ�ѧ���ۺ�֪ʶ��ע��֪ʶ�Ĺ��ɺ������ǹؼ����ѶȲ���

��ϰ��ϵ�д�
 ��У����ϵ�д�
��У����ϵ�д�
�����Ŀ