题目内容
设NA为阿伏加德罗常数,下列说法正确的是( )
| A.18gNH4+离子中所含的电子总数为12NA |
| B.标准状况下,11.2L水含有的分子数为0.5NA |
| C.1L0.3mol/LNa2SO4溶液中,含有Na+和SO42- 总数为0.9NA |
| D.常温常压下,铝从盐酸中置换出1molH2,电子转移的总数为3NA |
C
A选项18gNH4+物质的量为1mol,因为是带一个单位正电荷的阳离子,所以所含电子数应为10NA。B选项,标况下的水是固液混合状态,不能使用摩尔体积作为计算依据。C选项正确,Na2SO4在水溶液里是完全电离,且没有水解离子,所以应有0.6molNa+和0.3molSO42-,总数为0.9NA.D选项根据氧化还原反应中得失电子守恒,有1molH2被还原,说明H+得到电子为2NA,那么转移电子总数也应为2NA.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
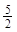 O2(g)→2CO2(g)+H2O(l);ΔH= -1300kJ/mol
O2(g)→2CO2(g)+H2O(l);ΔH= -1300kJ/mol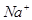 和
和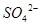 离子总数为0.9NA
离子总数为0.9NA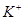 和
和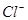 的物质的量浓度一定相同
的物质的量浓度一定相同