题目内容
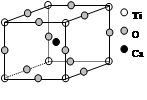
(1)水在不同的温度和压强条件下可以形成11种不同结构的晶体,密度从比水轻的0.92 g·cm-3到约为水的一倍半。冰是人们迄今已知的由一种简单分子堆积出结构花样最多的化合物。其中冰-Ⅶ的晶体结构为一个如下图所示的立方晶胞,每个水分子可与周围____________个水分子以氢键结合,晶体中,1 mol水可形成________ mol氢键。

(2)已知下列元素的电负性数据:H为2.1,O为3.5,F为4.0。OF2与水的立体结构相似,但水分子的极性比OF2强得多,其原因有:①OF2中氧原子上有两对孤对电子,抵消了F—O键中共用电子对偏向F而产生的极性;②从电负性上看,___________________________。

(2)已知下列元素的电负性数据:H为2.1,O为3.5,F为4.0。OF2与水的立体结构相似,但水分子的极性比OF2强得多,其原因有:①OF2中氧原子上有两对孤对电子,抵消了F—O键中共用电子对偏向F而产生的极性;②从电负性上看,___________________________。
(1)4 2
(2)氧与氢的电负性差大于氧与氟的电负性差
(2)氧与氢的电负性差大于氧与氟的电负性差
(1)观察图示的立方晶胞的中心水分子可知,该水分子与周围4个水分子以氢键结合;每2个水分子间形成的1个氢键,每个水分子只分得一半,故晶体中1 mol水可形成4 mol×0.5=2 mol氢键。(2)根据题中所给出的元素的电负性数据:H为2.1,O为3.5,F为4.0,氧与氢的电负性差(1.4)大于氧与氟的电负性差(0.5),因此,虽然OF2与水的立体结构相似,但水分子的极性比OF2强得多。

练习册系列答案
相关题目