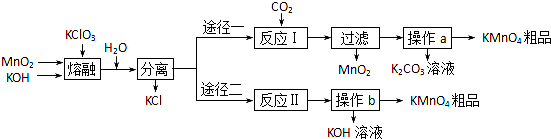
题目内容
Ⅰ.甲组用滴定法测定草酸晶体中结晶水的含量.
步骤一:称取5.0g纯净的草酸晶体,配制成250mL溶液.
步骤二:取0.04mol?L-1标准酸性KMnO4溶液25.00mL于锥形瓶中,用所配溶液滴定至终点.
请回答下列问题:
①配制草酸溶液的操作步骤依次是:将晶体置于烧杯中,加水溶解,将溶液转移入
②完善下面滴定反应的离子方程式:
③在“步骤一”和“步骤二”测定操作中需要重复进行的操作是
④其它操作均正确的情况下,下列操作可能使测定结果偏大的是
A.锥形瓶瓶壁残留蒸馏水就转移入酸性KMnO4溶液进行滴定
B.酸式滴定管用蒸馏水洗后未用待测溶液润洗就加入待测液进行滴定
C.滴定前酸式滴定管尖嘴处有气泡,滴定后气泡消失
D.滴定完成后俯视刻度
Ⅱ.乙组同学为探究草酸的性质,按下图所示装置进行实验(夹持装置未标出):
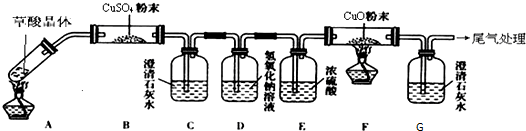
实验发现:装置C、G中澄清石灰水变浑浊,B中CuSO4粉末变蓝,F中CuO粉末部分变红.据此回答:
①草酸分解的化学方程式为
②乙组同学将B装置称量,却发现B装置质量增量比理论值大,该小组同学认真分析断定操作无误,则其原因可能是
③乙组中某同学认为可以利用加热分解的草酸晶体的质量和F装置中固体质量的减少就可以计算出晶体中结晶水的含量,立即遭到其他同学的反对,其反对的理由是
②分析反应前后元素化合价变化可知,Mn元素化合价从+7价变化为+2价,化合价降低做氧化剂,草酸中的碳元素化合价应升高,从+3价升高为+4价,所以以后产物为二氧化碳,依据电子守恒配平的离子方程式;
③步骤一是称量配制只需要一次准确操作,步骤二是滴定过程,为避免产生较大误差,滴定实验一般需要重复2-3次,所以测定操作中需要重复进行的操作是步骤二;
④依据滴定实验误差分析的依据是c(待测)=
| c(标准)×V(标准) |
| V(待测) |
Ⅱ,①依据实验装置过程中的反应现象分析草酸分解得到产物,结合原子守恒写出化学方程式;
②发现B装置质量增量比理论值大,该小组同学认真分析断定操作无误,依据草酸损耗的因素分析判断;
③依据利用加热分解的草酸晶体的质量和F装置中固体质量的减少就可以计算出晶体中结晶水的含量,实验设计分析,过程中产生误差的因素是生成的一氧化碳不能全部反应,试验时需要在整套装置中充满一氧化碳避免点燃时发生爆炸,草酸可能为全部分解,装置G中 液体倒流会装置F导致称量质量产生误差;
故答案为:250mL容量瓶;
②分析反应前后元素化合价变化可知,Mn元素化合价从+7价变化为+2价,化合价降低做氧化剂,草酸中的碳元素化合价应升高,从+3价升高为+4价,所以以后产物为二氧化碳,依据电子守恒配平的离子方程式为:2MnO4-+5H2C2O4+6H+=Mn2++10CO2↑+8H2O;
故答案为:2、5、6、2、10CO2↑、8;
③步骤一是称量配制只需要一次准确操作,步骤二是滴定过程,为避免产生较大误差,滴定实验一般需要重复2-3次,所以测定操作中需要重复进行的操作是步骤二;
故答案为:步骤二;
④A.锥形瓶瓶壁残留蒸馏水就转移入酸性KMnO4溶液进行滴定,对实验无影响,故A不符合;
B.酸式滴定管用蒸馏水洗后未用待测溶液润洗就加入待测液进行滴定,结构消耗标准液体积增大,结构偏高,故B符合;
C.滴定前酸式滴定管尖嘴处有气泡,滴定后气泡消失,滴定终点后读取标准液体积增大,测定浓度偏大,故C符合;
D.滴定完成后俯视刻度,读取的标准液体积减小,结构偏低,故D不符合;
故答案为:BC;
Ⅱ,①B中CuSO4粉末变蓝,说明分解产物含有水蒸气,装置C、G中澄清石灰水变浑浊,F中CuO粉末部分变红,证明生成的产物中含有二氧化碳气体和一氧化碳气体,依据原子守恒配平写出的化学方程式为:H2C2O4
| ||
故答案为:H2C2O4
| ||
②发现B装置质量增量比理论值大,该小组同学认真分析断定操作无误,说明草酸在加热分解过程中变成蒸气的在装置B的玻璃管内壁凝结
故答案为:在加热时草酸部分升华在B中部分凝华;
③依据利用加热分解的草酸晶体的质量和F装置中固体质量的减少就可以计算出晶体中结晶水的含量,实验设计分析,过程中产生误差的因素是生成的一氧化碳不能全部反应,试验时需要在整套装置中充满一氧化碳避免点燃时发生爆炸,草酸可能为全部分解,装置G中 液体倒流会装置F导致称量质量产生误差;
故答案为:前面的反应装置中滞留有大量CO气体;为防止爆炸在点燃F处酒精灯之前要先通一段时间的CO以排除装置系统中的空气;装置G中的水蒸气逆流进入装置F中;加热时草酸部分升华未能全部分解;

名称 | 分子式 | 颜色、状态 | 溶解性/g | 熔点/℃ | 密度/g·cm-3 |
乙二酸 | H2C2O4 | —— | 8.6(20℃) | 189.5 | 1.900 |
二水合乙二酸 | H2C2O4·2H2O | 无色晶体 | —— | 101.5 | 1.650 |
注:表中“——”表示尚未有具体数据。
回答下列问题:
(1)向盛有Na2CO3粉末的试管里加入约3 mL乙二酸溶液,观察到的现象为_____________;说明乙二酸的酸性比碳酸____________。
(2)向盛有5 mL乙二酸饱和溶液的试管中滴入3滴硫酸酸化的0.5%(质量分数)的KMnO4溶液,振荡,观察到现象为_______________________________________________________;说明乙二酸有______________________。
(3)向A试管中加入3 mL乙醇,然后,边振荡试管边加入2 mL 浓硫酸和2 mL乙二酸,按图甲连接好装置,加热3—5 min,在B试管中有油状、香味液体产生。该现象说明发生了______________(填有机反应类型)反应。在B试管中加入饱和Na2CO3溶液的目的是_______________________________________________________________。
导管在液面上的原因是________________________________________________。

(4)图乙是中学化学实验常用的装置,用此装置可制备的气体有___________(填标号)。
A.O2 B.H2 C.Cl2 D.NH3 E.CH2====CH2 F.CH![]() CH
CH
图乙试管口略低于试管底部的原因是_________________________________________。已知草酸分解的化学方程式为H2C2O4![]() H2O+CO2↑+CO↑。用图丙加热草酸晶体,验证草酸受热分解及其产物,图丙是中学化学教材中给出的实验装置图,但有人认为该装置不合理。请你根据草酸晶体的某些物理常数和实验目的,指出图丙不合理的原因。
H2O+CO2↑+CO↑。用图丙加热草酸晶体,验证草酸受热分解及其产物,图丙是中学化学教材中给出的实验装置图,但有人认为该装置不合理。请你根据草酸晶体的某些物理常数和实验目的,指出图丙不合理的原因。
答:______________________________________________________________。
该装置也不符合绿色化学的要求,因为________________________________________。