��Ŀ����
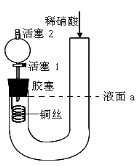
����Ŀ����.��1��������ͼ��ʾ������ж�����˵������ȷ���� ��

A�����Ȼ�ѧ����ʽΪ��CO(g) + H2O(g)=CO2(g) + H2(g) ��H��41 kJ��mol��1
B���÷�ӦΪ���ȷ�Ӧ
C���÷�ӦΪ���ȷ�Ӧ
D������H2OΪҺ̬ʱ��Ӧ��Ϊ��H2������H2����H
��2��25����101 kPa�£���֪1g������ȫȼ������Һ̬ˮʱ�ų�142.9 kJ����������ʾ����ȼ���ȵ��Ȼ�ѧ����ʽ�� ��
��3����֪��Ӧ��N2(g) + O2 (g) �� 2NO(g) ��H1
2H2(g) + O2(g) �� 2H2O(g) ��H2
N2(g) + 3H2(g) �� 2NH3(g) ��H3
��������������Ӧ������4NH3(g) + 5O2(g) �� 4NO(g) + 6H2O(g) ��H4 �ķ�Ӧ�ʱ�Ϊ (�ú���H1����H2����H3��ʽ�ӱ�ʾ)��
��4���⼰�仯�����ںϳ�ɱ������ҩ��ȷ�����й㷺��;���ش��������⣺
�������ĵ⸻���ں����У���ˮ��ȡ��Ũ��������Ũ��Һ�м�MnO2��H2SO4�����ɵõ�I2���÷�Ӧ�Ļ�ԭ����Ϊ ��
����֪��Ӧ2HI��g��![]() H2��g�� + I2��g������H= + 11kJmol��1��1molH2��g����1molI2��g�������л�ѧ������ʱ�ֱ���Ҫ����436KJ��151KJ����������1molHI��g�������л�ѧ������ʱ�����յ�����Ϊ kJ��
H2��g�� + I2��g������H= + 11kJmol��1��1molH2��g����1molI2��g�������л�ѧ������ʱ�ֱ���Ҫ����436KJ��151KJ����������1molHI��g�������л�ѧ������ʱ�����յ�����Ϊ kJ��
��Bodensteins�о������з�Ӧ��2HI��g��![]() H2��g�� + I2��g��
H2��g�� + I2��g��
��716Kʱ�����������е⻯������ʵ�������x��HI���뷴Ӧʱ��t�Ĺ�ϵ�����
t/min | 0 | 20 | 40 | 60 | 80 | 120 |
X��HI�� | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
X��HI�� | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
��������ʵ�������÷�Ӧ��ƽ�ⳣ��K�ļ���ʽΪ�� ��������Ӧ�У�����Ӧ����Ϊv��=k��x2��HI�����淴Ӧ����Ϊv��=k��x��H2��x��I2��������k����k��Ϊ���ʳ�������k��Ϊ ����K��k����ʾ������k��=0.0027min��1����t=40minʱ��v��= min��1��
���𰸡���1��B��2������2��H2(g) + 1/2 O2(g)��H2O��1�� ��H2=-285.8kJ��mol��1 ��2����
��3��2��H1 + 3��H2��2��H3 ��2���� MnSO4 299 ![]()
![]() 1.95��10��3
1.95��10��3
��������
�����������1��A������ͼ���֪��Ӧ���Ȼ�ѧ����ʽΪ��CO(g) + H2O(g)=CO2(g) + H2(g) ��H�� + 41 kJ��mol��1��A����B����Ӧ����������������������������÷�ӦΪ���ȷ�Ӧ��B��ȷ��C���÷�ӦΪ���ȷ�Ӧ��C����D������H2OΪҺ̬ʱ�ų��������࣬����Ӧ��Ϊ��H2������H2����H��D����ѡB��
��2��25����101 kPa�£���֪1g������ȫȼ������Һ̬ˮʱ�ų�142.9 kJ����������1mol������ȫȼ������Һ̬ˮʱ�ų�285.8kJ����������˱�ʾ����ȼ���ȵ��Ȼ�ѧ����ʽ��H2(g) + 1/2 O2(g)��H2O��1�� ��H2=-285.8kJ��mol��1��
��3����֪��Ӧ����N2(g) + O2 (g) �� 2NO(g) ��H1
��2H2(g) + O2(g) �� 2H2O(g) ��H2
��N2(g) + 3H2(g) �� 2NH3(g) ��H3
����ݸ�˹���ɿ�֪�١�2 + 3������2�������õ�4NH3(g) + 5O2(g)��4NO(g) + 6H2O(g) ��H4 �ķ�Ӧ�ʱ�Ϊ2��H1 + 3��H2��2��H3��
��4�����ⵥ��������������Ի�ԭ������MnSO4��
����H=E����Ӧ������ܺͣ���E������������ܺͣ�����1molHI��g�������л�ѧ������ʱ�����յ�����ΪxkJ��������㣺 + 11=2x����436 + 151�������x =299��
������Ӧǰ�����������ȣ���ͬ����ʼ̬�����״ﵽ��Ч��ƽ��״̬��ע�������е����������������������������ݡ�716Kʱ��ȡ��һ�����ݼ��㣺
2HI��g��![]() H2��g�� + I2��g��
H2��g�� + I2��g��
n��ʼ����ȡ1mol�� 1 0 0
��n 0.216 0.108 0.108
n��ƽ�� 0.784 0.108 0.108
��ѧƽ�ⳣ��Ϊ![]() ��
��
���ʵ�Ҫ������ƽ��״̬����v��= v����������k����x2(HI) = k����x(H2)��x(I2)��������k��/ k��=�� x(H2)��x(I2)��/ x2(HI)=K��������k��= k��/K��
����t��40minʱ������Ӧ����ƽ���x(HI)��0.85����v����k��x2(HI)��0.0027min-1��0.852��1.95��10-3min-1��

����Ŀ��Ԫ�����ڱ���Ԫ����������ѧϰ���о�������ʵ�����к���Ҫ�����á��±��г�������������Ԫ�������ڱ��е�λ�á�������صĻ�ѧ����ش��������⣺
�� | ��A | ��A | ��A | ��A | ��A | ��A | ��A[ | 0 |
2 | �� | �� | �� | |||||
3 | �� | �� | �� | �� | �� | |||
4 | �� |
��1�� ����ЩԪ���У�����õ��� �ǽ�������ǿ����___________,��������ǿ����___________;����Ԫ�ط��Ż�ѧʽ����ͬ����
��2�� ��ЩԪ���γɵ�����������Ӧ��ˮ�����м�����ǿ�� ��������ǿ��__________;
��3�� ������������������������Ԫ�ص�ԭ�Ӱ뾶�ɴ�С��˳��Ϊ ;
��4�� �����⻯��ĵ���ʽΪ ���� �ڿ�����ȼ�պ����ɲ���ĵ���ʽ ��