题目内容
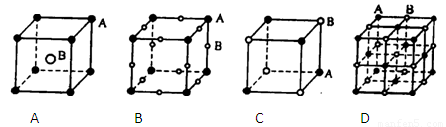
现有四种晶体,其离子排列方式如图所示,其中对应化学式正确的是( )
分析:利用均摊法计算晶胞中含有的离子个数,从而确定其化学式,顶点上的离子在每个晶胞中占
,面心上的离子在每个晶胞中占
,体心上的离子被一个晶胞占有.
| 1 |
| 8 |
| 1 |
| 2 |
解答:解:A.A离子个数是1,B离子个数=
×8=1,所以其化学式为AB,故A错误;
B.E离子个数=
×4=
,F离子个数=
×4=
,E、F离子个数比为
:
=1:1,所以其化学式为EF,故B错误;
C.X离子个数是1,Y离子个数=
×6=3,Z离子个数=
×8=1,所以其化学式为XY3Z,故C正确;
D.A离子个数=
×8+
×6=4,B离子个数=12×
+1=4,AB离子个数比为4:4=1:1,所以其化学式为AB,故D错误;
故选C.
| 1 |
| 8 |
B.E离子个数=
| 1 |
| 8 |
| 1 |
| 2 |
| 1 |
| 8 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
C.X离子个数是1,Y离子个数=
| 1 |
| 2 |
| 1 |
| 8 |
D.A离子个数=
| 1 |
| 8 |
| 1 |
| 2 |
| 1 |
| 4 |
故选C.
点评:本题考查了根据晶胞来确定化学式,根据均摊法来分析解答即可,难度不大.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目