题目内容
【题目】用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
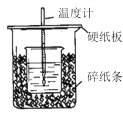
(1)从实验装置上看,图中尚缺少的一种玻璃用品是_____________________。
(2)烧杯间填满碎纸条的作用是_____________________。
(3)大烧杯上如不盖硬纸板,求得的中和热数值__________(填“偏大、偏小、无影响”)
(4)该同学所用的装置,有一处明显不合理,请你说明不合理之处:____________________。
(5)在实验过程中,该同学没有找到缺少的那一件用品,就用铁丝自己做了一个,你认为______(填“是、否)可以,请说明原因_____________________。
(6)实验中改用60 mL 0.50 mol·L-1的盐酸跟50 mL 0.55 mol·L-1的NaOH溶液进行反应,与上述实验相比,所求中和热_________ (填“相等”或“不相等”),所放出的热量_________(填“相等”或“不相等”)。
(7)用相同浓度和体积的醋酸(CH3COOH)代替盐酸溶液进行上述实验,测得的中和热的数值会___________;(填“偏大”、“偏小”、“无影响”)。
【答案】 环形玻璃搅拌棒 减少实验过程中的热量损失 偏小 两烧杯口没有在同一水平面 否 铁是热的良导体,用铁丝作搅拌棒,会增大实验误差 相等 不相等 偏小
【解析】考查中和热的测定,△H=-cm(t1-t0)/n(H2O),(1)根据中和热的测定,缺少的玻璃仪器是环形玻璃搅拌棒;(2)中和热的测定,需要减少热量损失,因此碎纸条的目的保温,减少实验过程中的热量损失;(3)大烧杯上如不盖硬纸板,造成热量损失,t1减少,因此中和热数值减小;(4)两烧杯口没有在同一水平面,造成热量损失,所测数值偏小;(5)铁丝是热的良导体,造成热量损失,即铁是热的良导体,用铁丝作搅拌棒,会增大实验误差,因此不能用铁丝代替环形玻璃搅拌棒;(6)中和热是稀酸和稀碱反应生成1molH2O时放出的热量,与所加物质的量无关,即中和热相等,放出热量不相等;(7)醋酸是弱电解质,电离吸收热量,造成所测中和热数值偏小。