题目内容
pH=1的两种一元酸HX与HY溶液,分别取50 mL加入足量的镁粉,充分反应后,收集到H2体积分别为V(HX)和V(HY)。若V(HX)>V(HY),则下列说法正确的是
A.HX可能是强酸
B.HX的酸性比HY的酸性弱
C.两酸的浓度大小[HX]<[HY]
D.pH=1的两种一元酸均稀释100倍,稀释后两溶液的pH均为3
【答案】
B
【解析】
试题分析:pH=1的两种一元酸HX与HY溶液中氢离子的浓度相等,在溶液体积相等的条件下,与足量镁反应产生的氢气体积是V(HX)>V(HY),这说明HX一定是弱酸,HY可能是强酸或弱酸,所以选项A不正确,B正确;由于弱酸存在电离平衡,则反应前两酸的浓度大小[HX]>[HY],C不正确;弱酸在稀释过程中促进电离,因此pH=1的两种一元酸均稀释100倍,稀释后两溶液的pH≤3,D不正确,答案选B。
考点:考查弱酸的电离平衡、外界条件对电离平衡的影响以及溶液pH计算等

练习册系列答案
相关题目
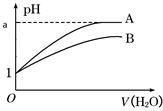
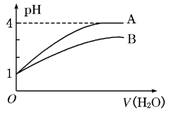
常温下pH=1的两种一元酸溶液A和B,分别加水稀释至1000倍,其pH与所加水的体积变化如图所示,则下列结论中一定正确的是 ( )
| A.A酸比B酸的电离程度小 |
| B.A是强酸,B是弱酸 |
| C.pH=1时,B酸的物质的量浓度比A酸大 |
| D.将pH=1的A酸和B酸稀释成pH=5的溶液,A酸所需加入的水量多 |