题目内容
(6分)用NaOH与Na2CO3·nH2O的混合物共28 g配制成100 mL溶液,测得该溶液中c(Na+)=4 mol·L-1。另取相同质量的上述混合物,加入足量的盐酸完全反应后,放出的气体在标准状况下的体积为3.36 L,试计算:
(1)原混合物中NaOH的质量分数。(2)Na2CO3·nH2O中的n值。
(1)原混合物中NaOH的质量分数。(2)Na2CO3·nH2O中的n值。
原混合物中NaOH的质量分数为14.3 %,Na2CO3·nH2O中n等于3。
解法Ⅰ:
(1)Na2CO3+2HCl===2NaCl+CO2↑+H2O
1 mol 22.4 L
n(Na2CO3) 3.36 L
n(Na2CO3)==0.15 mol,由题意得 n(Na+)=2n(Na2CO3)+n(NaOH)=4 mol·L-1×0.1 L=0.4 mol
所以n(NaOH)=0.4 mol-0.3 mol=0.1 mol,w(NaOH)=×100%=14.3%
(2)28 g混合物中Na2CO3·nH2O的质量为28 g-m(NaOH)=28 g-0.1 mol×40 g·mol-1=24 g
其中m(Na2CO3)=0.15 mol×106 g·mol-1=15.9 g,= n=3
答:原混合物中NaOH的质量分数为14.3 %,Na2CO3·nH2O中n等于3。
解法Ⅱ:(1)n(Na2CO3)=n(CO2)==0.15 mol
n(NaOH)=4 mol·L-1×0.1 L-2×0.15 mol=0.1 mol,w(NaOH)=×100 %=14.3 %
(2)结晶水合物中结晶水的质量m(H2O)=28 g-m(NaOH)-m(Na2CO3)=28 g-0.1 mol×40 g·mol-1-0.15 mol×106 g·mol-1=8.1 g,n(H2O)==0.45 mol,结晶水合物Na2CO3·nH2O中 n===3。
(1)Na2CO3+2HCl===2NaCl+CO2↑+H2O
1 mol 22.4 L
n(Na2CO3) 3.36 L
n(Na2CO3)==0.15 mol,由题意得 n(Na+)=2n(Na2CO3)+n(NaOH)=4 mol·L-1×0.1 L=0.4 mol
所以n(NaOH)=0.4 mol-0.3 mol=0.1 mol,w(NaOH)=×100%=14.3%
(2)28 g混合物中Na2CO3·nH2O的质量为28 g-m(NaOH)=28 g-0.1 mol×40 g·mol-1=24 g
其中m(Na2CO3)=0.15 mol×106 g·mol-1=15.9 g,= n=3
答:原混合物中NaOH的质量分数为14.3 %,Na2CO3·nH2O中n等于3。
解法Ⅱ:(1)n(Na2CO3)=n(CO2)==0.15 mol
n(NaOH)=4 mol·L-1×0.1 L-2×0.15 mol=0.1 mol,w(NaOH)=×100 %=14.3 %
(2)结晶水合物中结晶水的质量m(H2O)=28 g-m(NaOH)-m(Na2CO3)=28 g-0.1 mol×40 g·mol-1-0.15 mol×106 g·mol-1=8.1 g,n(H2O)==0.45 mol,结晶水合物Na2CO3·nH2O中 n===3。

练习册系列答案
 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案
相关题目
 2H2↑+O2↑,2H2+O2
2H2↑+O2↑,2H2+O2 2H2O
2H2O NH3↑+H2O↑+CO2↑
NH3↑+H2O↑+CO2↑ CuO2AgBr,2AgBr
CuO2AgBr,2AgBr 2Ag+Br2
2Ag+Br2 8Cu+4FeO+2Fe2O3+16SO2,下列有关说法不正确的是( )
8Cu+4FeO+2Fe2O3+16SO2,下列有关说法不正确的是( )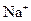
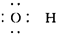 ]-
]-