题目内容
(2011?福建)四氯化钛(TiCl4)是制取航天航空工业材料--钛合金的重要原料,由钛铁矿(主要成分是FeTiO3)制备TiCl4等产品的一种工艺流程示意如下:

回答下列问题:
(1)往①中加入铁屑至浸出液显紫色,此时溶液仍呈强酸性.该过程中有如下反应发生.
2Fe3++Fe═3Fe2+
2TiO2+(无色)+Fe+4H+═2Ti3+(紫色)+Fe2++2H2O
Ti3+(紫色)+Fe3++H2O═TiO2+(无色)+Fe2++2H+
加入铁屑的作用是
(2)在②→③工艺中需要控制条件以形成TiO2?nH2O溶胶,该分散质颗粒直径大小在
(3)若把③中制得的固体TiO2?nH2O用酸清洗除去其中的Fe(OH)3杂质,还可制得钛白粉.已知25℃时,Ksp[Fe(OH)3]=2.79×10-39,该温度下反应Fe(OH)3+3H+?Fe3++H2O的平衡常数K=
(4)已知:TiO2(s)+2Cl2(g)═TiCl4(l)+O2(g)△H=+140kJ?mol-1;2C(s)+O2(g)═2CO(g)△H=-221kJ?mol-1
写出④中TiO2和焦炭、氯气反应生成液态TiCl4和CO气体的热化学方程式:
(5)上述工艺具有成本低、可用低品位矿物为原料等优点.依据绿色化学理念,该工艺流程中存在的不足之处是
(6)依据如表信息,要精制含少量SiCl4杂质的TiCl4,可采用

回答下列问题:
(1)往①中加入铁屑至浸出液显紫色,此时溶液仍呈强酸性.该过程中有如下反应发生.
2Fe3++Fe═3Fe2+
2TiO2+(无色)+Fe+4H+═2Ti3+(紫色)+Fe2++2H2O
Ti3+(紫色)+Fe3++H2O═TiO2+(无色)+Fe2++2H+
加入铁屑的作用是
防止Ti3+被Fe3+氧化成TiO2+
防止Ti3+被Fe3+氧化成TiO2+
.(2)在②→③工艺中需要控制条件以形成TiO2?nH2O溶胶,该分散质颗粒直径大小在
1nm-100nm
1nm-100nm
范围.(3)若把③中制得的固体TiO2?nH2O用酸清洗除去其中的Fe(OH)3杂质,还可制得钛白粉.已知25℃时,Ksp[Fe(OH)3]=2.79×10-39,该温度下反应Fe(OH)3+3H+?Fe3++H2O的平衡常数K=
2.79×103
2.79×103
.(4)已知:TiO2(s)+2Cl2(g)═TiCl4(l)+O2(g)△H=+140kJ?mol-1;2C(s)+O2(g)═2CO(g)△H=-221kJ?mol-1
写出④中TiO2和焦炭、氯气反应生成液态TiCl4和CO气体的热化学方程式:
TiO2(s)+2C(s)+2Cl2 (g)=TiCl4(l)+2CO(g)△H=-81KJ?mol-1
TiO2(s)+2C(s)+2Cl2 (g)=TiCl4(l)+2CO(g)△H=-81KJ?mol-1
.(5)上述工艺具有成本低、可用低品位矿物为原料等优点.依据绿色化学理念,该工艺流程中存在的不足之处是
产生了废气,废液,废渣等
产生了废气,废液,废渣等
(只要求写出一项).(6)依据如表信息,要精制含少量SiCl4杂质的TiCl4,可采用
蒸馏(或分馏)等方法
蒸馏(或分馏)等方法
方法.| TiCl4 | SiCl4 | |
| 熔点/℃ | -25.0 | -68.8 |
| 沸点/℃ | 136.4 | 57.6 |
分析:(1)往①中加入铁屑至浸出液显紫色,说明浸出液中含有Ti3+,由方程式可知,Fe3+氧化为Ti3+;
(2)控制条件以形成TiO2?n H2O溶胶,说明得到胶体,其分散质颗粒直径大小为10-9~10-7m(或1nm-100nm);
(3)依据平衡常数的概念结合反应写出计算式计算平衡浓度得到;
(4)依据热化学方程式和盖斯定律计算分析得到;
(5)绿色化学应零污染、零排放,原子利用率100%.结合工艺流程三废回答;
(6)由表中数据可知,SiCl4、TiCl4为液体,二者沸点相差较大,通常采取蒸馏方法分离.
(2)控制条件以形成TiO2?n H2O溶胶,说明得到胶体,其分散质颗粒直径大小为10-9~10-7m(或1nm-100nm);
(3)依据平衡常数的概念结合反应写出计算式计算平衡浓度得到;
(4)依据热化学方程式和盖斯定律计算分析得到;
(5)绿色化学应零污染、零排放,原子利用率100%.结合工艺流程三废回答;
(6)由表中数据可知,SiCl4、TiCl4为液体,二者沸点相差较大,通常采取蒸馏方法分离.
解答:解:(1)往①中加入铁屑至浸出液显紫色,说明浸出液中含有Ti3+,由方程式可知,Fe3+氧化为Ti3+,加入铁屑作还原剂,将Fe3+还原为Fe2+,防止Ti3+被Fe3+氧化成TiO2+,
故答案为:防止Ti3+被Fe3+氧化成TiO2+;
(2)控制条件以形成TiO2?n H2O溶胶,说明得到胶体,其分散质颗粒直径大小为10-9~10-7m(或1nm-100nm),
故答案为:10-9~10-7m(或1nm-100nm);
(3)Ksp[Fe(OH)3]=c(Fe3+)×c3(OH-)=2.79×10-39,反应Fe (OH)3+3H+?Fe3++H2O的平衡常数K=
=
=c(Fe3+)×c3(OH-)×1042=2.79×10-39×1042=2.79×103.
故答案为:2.79×103;
(4)①TiO2 (s)+2Cl2 (g)═TiCl4(l)+O2(g)△H=+140KJ?mol-1
②2C(s)+O2(g)═2CO(g)△H=-221KJ?mol-1
依据盖斯定律①+②得到:TiO2(s)+2C(s)+2Cl2 (g)=TiCl4(l)+2CO(g)△H=-81KJ?mol-1;
故答案为:TiO2(s)+2C(s)+2Cl2 (g)=TiCl4(l)+2CO(g)△H=-81KJ?mol-1
(5)由工艺流程可知,生成中产生废气,废液,废渣等,不符合绿色化学理念,
故答案为:产生了废气,废液,废渣等;
(6)由表中数据可知,SiCl4、TiCl4为液体,二者沸点相差较大,要精制含少量SiCl4杂质的TiCl4,可采用蒸馏(或分馏)方法,
故答案为:蒸馏(或分馏);
故答案为:防止Ti3+被Fe3+氧化成TiO2+;
(2)控制条件以形成TiO2?n H2O溶胶,说明得到胶体,其分散质颗粒直径大小为10-9~10-7m(或1nm-100nm),
故答案为:10-9~10-7m(或1nm-100nm);
(3)Ksp[Fe(OH)3]=c(Fe3+)×c3(OH-)=2.79×10-39,反应Fe (OH)3+3H+?Fe3++H2O的平衡常数K=
| c(Fe3+) |
| c3(H+) |
| c(Fe3+) | ||
(
|
故答案为:2.79×103;
(4)①TiO2 (s)+2Cl2 (g)═TiCl4(l)+O2(g)△H=+140KJ?mol-1
②2C(s)+O2(g)═2CO(g)△H=-221KJ?mol-1
依据盖斯定律①+②得到:TiO2(s)+2C(s)+2Cl2 (g)=TiCl4(l)+2CO(g)△H=-81KJ?mol-1;
故答案为:TiO2(s)+2C(s)+2Cl2 (g)=TiCl4(l)+2CO(g)△H=-81KJ?mol-1
(5)由工艺流程可知,生成中产生废气,废液,废渣等,不符合绿色化学理念,
故答案为:产生了废气,废液,废渣等;
(6)由表中数据可知,SiCl4、TiCl4为液体,二者沸点相差较大,要精制含少量SiCl4杂质的TiCl4,可采用蒸馏(或分馏)方法,
故答案为:蒸馏(或分馏);
点评:本题考查学生阅读题目获取信息能力、氧化还原反应、绿色化学、胶体、物质分离提纯,平衡常数计算,溶度积常数的计算应用,盖斯定律的计算应用等,难度不大,注意基础知识的掌握利用.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
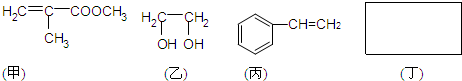

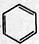 +CH3CH2Cl
+CH3CH2Cl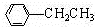 +HCl
+HCl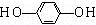
 (2011?福建模拟)A~D是含有同一元素的四种物质,相互之间有如图所示的转化关系,其中A既可为单质.又可为气态氢化物,D是最高价氧化物的水化物,则A、B、C、D中共同含有的元素是( )
(2011?福建模拟)A~D是含有同一元素的四种物质,相互之间有如图所示的转化关系,其中A既可为单质.又可为气态氢化物,D是最高价氧化物的水化物,则A、B、C、D中共同含有的元素是( )