题目内容
【题目】20℃时,饱和NaCl溶液的密度为ρ g·cm3,物质的量浓度为c mol/L,则下列说法中不正确的是 ( )
A. 温度低于20 ℃时,饱和NaC1溶液的浓度小于c mol/L
B. 此溶液中NaCl的质量分数为![]() ×100%
×100%
C. 将1 L该NaCl溶液蒸干可得到58.5c gNaCl固体
D. 20 ℃时,NaCl的溶解度S=![]() g
g
【答案】D
【解析】
A. 温度降低,氯化钠的溶解度减小,溶液中氯化钠的物质的量浓度减小;
B.根据c=![]() 可以知道,w=
可以知道,w=![]() 100%,据此解答;
100%,据此解答;
C.根据n=cV,m=nM计算溶质氯化钠的质量;
D. 设溶液体积为1L,根据氯化钠密度、浓度及溶解度表达式计算出该温度下的溶解度。
A. 温度低于20℃时,氯化钠饱和溶液中溶解的氯化钠减少,所以饱和NaCl溶液的浓度小于c mol/L,所以A选项是正确的;
B. 根据c=![]() 可以知道,w=
可以知道,w=![]() 100%=
100%=![]() ×100%,所以B选项是正确的;
×100%,所以B选项是正确的;
C. 1 Lc mol/LNaCl溶液中,n(NaCl)=cmol,m(NaCl)=58.5cg,则蒸干可得到58.5c gNaCl固体,所以C选项是正确的;
D. 20℃时,1L饱和NaCl溶液中溶解的氯化钠的质量为58.5cg,溶液质量为100![]() ,则该温度下氯化钠的溶解度为:S=
,则该温度下氯化钠的溶解度为:S=![]() 100g=
100g=![]() g,故D错误。
g,故D错误。
故选D。

 阅读快车系列答案
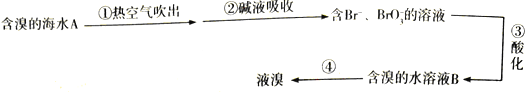
阅读快车系列答案【题目】2016年度国家科学技术奖授予我国诺贝尔奖获得者屠呦呦,以表彰她在抗疟疾青蒿素方面的研究。
【查阅资料】青蒿素为无色针状晶体,熔点156~157℃,易溶于丙酮、氯仿和苯,在水几乎不溶。
I.实验室用乙醚提取青蒿素的工艺流程如下:

(1)在操作I前要对青蒿进行粉碎,其目的是__________________。
(2)操作II的名称是_____________。
(3)操作III进行的是重结晶,其操作步骤为__________________________。
II.已知青蒿素是一种烃的含氧衍生物,为确定的化学式,有进行了如下实验:
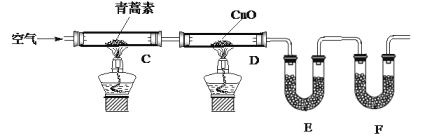
实验步骤:
①连接装置,检查装置的气密性。
② 称量E、F中仪器及药品的质量
③取14.10g青蒿素放入硬质试管C中,点燃C、D处酒精灯加热,充分燃烧
④实验结束后冷却至室温,称量反应后E、F中仪器及药品的质量
(4)装置E、F应分别装入的药品为_______________、___________________。
(5)实验测得:
装置 | 实验前 | 实验后 |
E | 24.00g | 33.90g |
F | 100.00g | 133.00g |
通过质谱法测得青蒿素的相对分子质量为282,结合上述数据,得出青蒿素的分子式为______。
(6)若使用上述方法会产生较大实验误差,你的改进方法是________________________。