题目内容
某一氯代烷1.85 g,与足量的NaOH水溶液混合加热后,用硝酸酸化,再加入足量AgNO3溶液,生成白色沉淀2.87 g。(1)通过计算,写出这种一氯代烷的各种同分异构体的结构简式。
(2)若此一氯代烷与足量NaOH溶液共热后,不经硝酸酸化就加AgNO3溶液,将会产生什么现象?写出有关的化学反应方程式。
(3)能否用硝酸银溶液直接与卤代烃反应来鉴别卤代烷?为什么?
解析:(1)一氯代烷的通式为CnH2n+1Cl,有关反应的方程式为:
CnH2n+1Cl+H2O![]() CnH2n+1OH+HCl
CnH2n+1OH+HCl
HCl+NaOH![]() NaCl+H2O
NaCl+H2O
NaOH+HNO3![]() NaNO3+H2O
NaNO3+H2O
NaCl+AgNO3![]() AgCl↓+NaNO3
AgCl↓+NaNO3
则CnH2n+1Cl — AgCl
14n+36.5 143.5
1 .85 g 2.87 g
![]() n=4
n=4
故一氯代烷的分子式为C4H9Cl,其同分异构体的可能结构有:
![]()
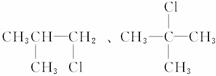
(2)若C4H9Cl与NaOH水溶液共热后不经硝酸酸化就加AgNO3溶液,将会产生褐色沉淀。因为过量的NaOH能与AgNO3反应生成白色的AgOH沉淀,但AgOH不稳定,马上分解为褐色Ag2O,有关反应的化学方程式为:
AgNO3+NaOH![]() AgOH↓+NaNO3
AgOH↓+NaNO3
2AgOH![]() Ag2O+H2O
Ag2O+H2O
AgNO3+NaCl![]() AgCl↓+NaNO3
AgCl↓+NaNO3
答案:(1)
![]()
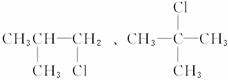
(2)将会产生褐色沉淀
AgNO3+NaOH![]() AgOH↓+NaNO3
AgOH↓+NaNO3
2AgOH![]() Ag2O+H2O
Ag2O+H2O
AgNO3+NaCl![]() AgCl↓+NaNO3
AgCl↓+NaNO3
(3)不能,因卤代烃中的卤素均是以卤原子的形式与碳原子结合着的,不能与Ag+反应。

练习册系列答案
相关题目
 ,生成白色沉淀2.87 g。试通过计算确定该一氯代烷的分子式,并写出各种同分异构体的结构简式。
,生成白色沉淀2.87 g。试通过计算确定该一氯代烷的分子式,并写出各种同分异构体的结构简式。