题目内容
在一密闭的2L容器里装有4molSO2和2molO2,在一定条件下开始反应。2min末测得容器中有1.6mol SO2 。
请计算①2min末SO3的浓度;
②2min内O2的平均反应速率。
(10分,每问5分) ① 1.2mol/L ② 0.3mol/(L·min)
解析试题分析: 2SO2+O2 2SO3
2SO3
起始浓度(mol/L) 2 1 0
转化浓度(mol/L) 1.2 0.6 1.2
2min后浓度(mol/L)0.8 0.4 1.2
所以2min末SO3的浓度是1.2mol/L
2min内O2的平均反应速率是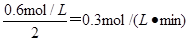
考点:考查可逆反应的有关计算
点评:该题是高考中的常见题型,属于中等难度的试题。试题基础性强,侧重对学生解题能力的培养,有助于培养学生的规范答题能力,提高学生灵活运用基础知识解决实际问题的能力。该类试题需要注意的是在进行可逆反应的有关计算时,一般采用“三段式”进行,即分别列出起始量、转化量和平衡量或某深刻的量,然后依据已知条件列式计算即可。

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目