题目内容
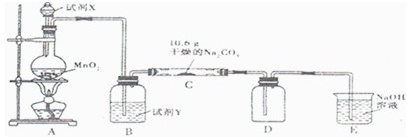
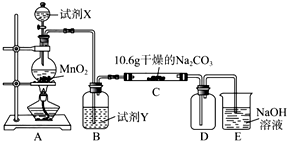
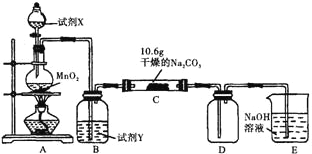
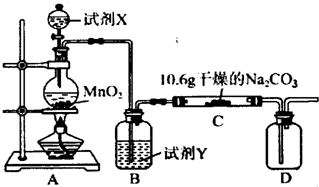
某化学活动小组设计如图所示(部分夹持装置已略去)实验装置,以探究潮湿的Cl2与Na2CO3反应得到的固体物质的成分.
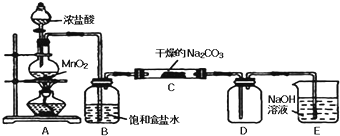
(1)写出装置A中发生反应的化学方程式: .
(2)装置B的主要作用是 .
(3)向C装置中通入一定量的氯气后,测得只生成一种气体(常温下为红黄色,且为氯的氧化物).可以确定的是C得到的固体最多含有三种物质,含有氯元素的盐只有一种,且含有NaHCO3,现对C中得到的固体成分进行猜想和验证.
①提出合理猜想
一定含有NaHCO3和 ;可能含有剩余的Na2CO3.
②设计方案,进行成分检验.请完成实验步骤3、4以及预期现象和结论
限选实验试剂:蒸馏水、稀HNO3、BaCl2溶液、澄清石灰水、AgNO3溶液、品红、稀盐酸.
(4)完成C中反应的化学方程式:2Cl2+2Na2CO3+H2O= .

(1)写出装置A中发生反应的化学方程式:
(2)装置B的主要作用是
(3)向C装置中通入一定量的氯气后,测得只生成一种气体(常温下为红黄色,且为氯的氧化物).可以确定的是C得到的固体最多含有三种物质,含有氯元素的盐只有一种,且含有NaHCO3,现对C中得到的固体成分进行猜想和验证.
①提出合理猜想
一定含有NaHCO3和
②设计方案,进行成分检验.请完成实验步骤3、4以及预期现象和结论
限选实验试剂:蒸馏水、稀HNO3、BaCl2溶液、澄清石灰水、AgNO3溶液、品红、稀盐酸.
| 实验步骤 | 预期现象和结论 |
| 步骤1:取C中的少量固体样品于试管中,加入蒸馏水至固体溶解,然后各取1~2mL所得溶液分别置于甲、乙两支试管中. | 得到无色溶液 |
| 步骤2:向甲试管中加入过量的BaCl2溶液,静置 | 若溶液变浑浊,证明固体中含碳酸钠. |
| 步骤3: |
|
| 步骤4: |
分析:(1)二氧化锰与浓盐酸反应生成氯化镁、氯气、水;
(2)氯气中混有挥发的HCl;
(3)①氯气和碳酸钠反应,由元素守恒可知一定会生成NaCl;
②澄清石灰水与碳酸氢钠反应生成碳酸钙沉淀;NaCl与硝酸银反应生成氯化银白色沉淀;
(4)由(3)可知,生成NaHCO3、NaCl,还生成一种气体为氯的氧化物,由电子守恒及质量守恒定律分析.
(2)氯气中混有挥发的HCl;
(3)①氯气和碳酸钠反应,由元素守恒可知一定会生成NaCl;
②澄清石灰水与碳酸氢钠反应生成碳酸钙沉淀;NaCl与硝酸银反应生成氯化银白色沉淀;
(4)由(3)可知,生成NaHCO3、NaCl,还生成一种气体为氯的氧化物,由电子守恒及质量守恒定律分析.
解答:解:(1)二氧化锰与浓盐酸反应生成氯化镁、氯气、水,该反应为MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,故答案为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O;
(2)氯气中混有挥发的HCl,则装置B为除杂装置,其作用为除去Cl2中混有的HCl气体,故答案为:除去Cl2中混有的HCl气体;
(3)①氯气和碳酸钠反应时,可看成氯气和水反应生成HCl、HClO,再与Na2CO3反应,由元素守恒可知一定会生成NaCl,故答案为:NaCl;
②因澄清石灰水与碳酸氢钠反应生成碳酸钙沉淀,NaCl与硝酸银反应生成氯化银白色沉淀,则步骤3为向甲中上层清液中滴入少量澄清石灰水,现象和结论为若上层清液变浑浊,证明固体中含有碳酸氢钠;步骤4为向乙试管中加入过量的稀HNO3,再滴入少量AgNO3溶液,现象与结论为若生成白色沉淀,证明固体中含有氯化钠,
故答案为:
(4)由(3)可知,生成NaHCO3、NaCl,还生成一种气体为氯的氧化物X,由2Cl2+2Na2CO3+H2O=2NaHCO3+2NaCl+X可知,由电子守恒可知X中Cl元素的化合价为+1价,由原子守恒可知X中含2个Cl、1和O,即X为Cl2O,该反应为2Cl2+2Na2CO3+H2O=2NaHCO3+2NaCl+Cl2O↑,故答案为:2NaHCO3+2NaCl+Cl2O↑.
| ||
| ||
(2)氯气中混有挥发的HCl,则装置B为除杂装置,其作用为除去Cl2中混有的HCl气体,故答案为:除去Cl2中混有的HCl气体;
(3)①氯气和碳酸钠反应时,可看成氯气和水反应生成HCl、HClO,再与Na2CO3反应,由元素守恒可知一定会生成NaCl,故答案为:NaCl;
②因澄清石灰水与碳酸氢钠反应生成碳酸钙沉淀,NaCl与硝酸银反应生成氯化银白色沉淀,则步骤3为向甲中上层清液中滴入少量澄清石灰水,现象和结论为若上层清液变浑浊,证明固体中含有碳酸氢钠;步骤4为向乙试管中加入过量的稀HNO3,再滴入少量AgNO3溶液,现象与结论为若生成白色沉淀,证明固体中含有氯化钠,
故答案为:
| 实验步骤 | 预期现象和结论 |
| 步骤3:向甲中上层清液中滴入少量澄清石灰水 | 若上层清液变浑浊,证明固体中含有碳酸氢钠 |
| 步骤4:向乙试管中加入过量的稀HNO3,再滴入少量AgNO3溶液 | 若生成白色沉淀,证明固体中含有氯化钠 |
点评:本题以探究潮湿的Cl2与Na2CO3反应得到的固体物质的成分考查氯气的制法及离子的检验,综合性较强,把握常见离子的检验方法、物质的性质、质量守恒定律等为解答的关键,注重基础知识的迁移应用,题目难度中等.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目