题目内容
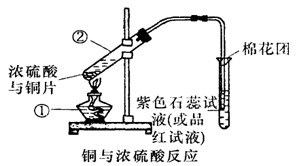
如图是铜与浓硫酸反应的实验装置图.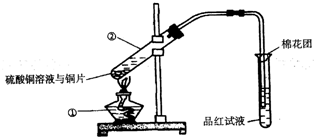
请回答下列问题:
(1)写出有标号仪器的名称:①
(2)写出铜与浓硫酸反应的化学方程式:
(3)过量SO2通入品红溶液中的现象是:
分析:(1)由实验装置图可知①②仪器的名称;
(2)浓硫酸和铜在加热的条件下生成硫酸铜、二氧化硫和水;
(3)SO2具有漂白性,可以使品红溶液褪色,SO2的漂白是暂时性的漂白;
(2)浓硫酸和铜在加热的条件下生成硫酸铜、二氧化硫和水;
(3)SO2具有漂白性,可以使品红溶液褪色,SO2的漂白是暂时性的漂白;
解答:解:(1)由实验装置图可知①是酒精灯,②是硬质大试管,
故答案为:酒精灯;试管;
(2)浓硫酸和铜在加热的条件下生成硫酸铜、二氧化硫和水,化学方程式为:Cu+2H2SO4(浓)
CuSO4+2H2O+SO2↑,
故答案为:Cu+2H2SO4(浓)
CuSO4+2H2O+SO2↑;
(3)SO2具有漂白性,可以使品红溶液褪色,但是SO2的漂白是暂时性的漂白,属于化合型漂白,生成的物质不稳定,受热易分解,溶液重新变为红色,
故答案为:褪色;又变为红色.
故答案为:酒精灯;试管;
(2)浓硫酸和铜在加热的条件下生成硫酸铜、二氧化硫和水,化学方程式为:Cu+2H2SO4(浓)
| ||
故答案为:Cu+2H2SO4(浓)
| ||
(3)SO2具有漂白性,可以使品红溶液褪色,但是SO2的漂白是暂时性的漂白,属于化合型漂白,生成的物质不稳定,受热易分解,溶液重新变为红色,
故答案为:褪色;又变为红色.
点评:本题考查浓硫酸和二氧化硫的性质,涉及浓硫酸的强氧化性和二氧化硫的漂白性、还原性,注意二氧化硫漂白性与氧化型漂白、吸附性漂白的区别,整体比较基础,难度不大.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
 已知:Cu+2H2SO4(浓)
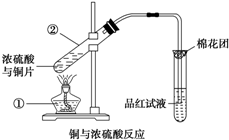
已知:Cu+2H2SO4(浓)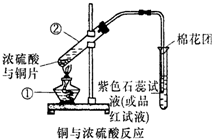 如图是铜与浓硫酸反应的实验装置图,请回答下列问题.
如图是铜与浓硫酸反应的实验装置图,请回答下列问题.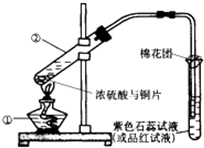 如图是铜与浓硫酸反应的实验装置图,请回答下列问题.
如图是铜与浓硫酸反应的实验装置图,请回答下列问题. CuSO4+SO2↑+2H2O,如图是铜与浓硫酸反应的实验装置图,请回答下列问题。
CuSO4+SO2↑+2H2O,如图是铜与浓硫酸反应的实验装置图,请回答下列问题。