题目内容
环境监测测定水中溶解O2的方法是:量取amL水样迅速加入MnSO4溶液及含有NaOH的KI溶液,立即塞好塞子,振荡使反应均匀,开塞,迅速加入适量H2SO4,此时有I2生成,用Na2S2O3溶液(浓度为bmol·L-1)和I2反应,消耗了VmL(以淀粉为指示剂)有关反应的离子方程式为 2Mn2++O2+4OH- ![]() 2MnO(OH)2(反应快)
2MnO(OH)2(反应快)
MnO(OH)2+2I-+4H+ ![]() Mn2++I2+3H2O
Mn2++I2+3H2O
I2+2![]()
![]() 2I-+
2I-+![]()
(1)水中溶解O2的量(以mg·L-1为单位)为多少?
(2)I2和![]() 反应以淀粉为指示剂,达到终点时溶液的颜色如何变化?
反应以淀粉为指示剂,达到终点时溶液的颜色如何变化?
(3)加MnSO4及含NaOH的KI溶液后振荡时,若塞子未塞紧(设振荡时未溅出溶液),测定结果与(1)中的计算结果相比有差别吗?为什么?
(4)开塞到加H2SO4前的时间间隔很长,测定结果又如何?说明理由。
解析:这是一道信息给予题,已知量为Na2S2O3的物质的量,未知量为溶解在水中的O2的量,根据题给条件找出O2与Na2S2O3之间的量的关系是解答此题的关键,由题中三个离子方程式可得关系式:O2~4Na2S2O3,据此可进行计算。
(1)O2~4Na2S2O3
1mol 4mol
n(O2) V×10
![]()
![]()
因此水中溶解氧气的量为
![]()
(2)I2与![]() 反应以淀粉为指示剂,在含I2的溶液中加入淀粉后溶液变蓝色,这个过程是可逆的,向溶液中加入Na2S2O3溶液与I2发生反应,当I2刚好被消耗完后,溶液由蓝色变为无色。
反应以淀粉为指示剂,在含I2的溶液中加入淀粉后溶液变蓝色,这个过程是可逆的,向溶液中加入Na2S2O3溶液与I2发生反应,当I2刚好被消耗完后,溶液由蓝色变为无色。
(3)若塞子未塞紧,水中溶解的O2反应消耗完后,空气中的O2又会溶解,这样会引起测定结果的偏高。
(4)若开塞到加H2SO4前的时间间隔很长,由于溶解的O2消耗完后,空气中的O2也会溶解,从而导致测定结果偏高。
![]()
(2)向含淀粉的I2溶液中加入Na2S2O3溶液,达到终点时,溶液颜色由蓝色变为无色。
(3)偏高,空气中的O2溶解。
(4)偏高,空气中的O2溶解。

 名校课堂系列答案
名校课堂系列答案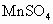 及含有NaOH的KI溶液,塞好塞子,振荡使反应均匀后,开塞,迅速加入硫酸,此时有碘生成,用浓度为bmol·
及含有NaOH的KI溶液,塞好塞子,振荡使反应均匀后,开塞,迅速加入硫酸,此时有碘生成,用浓度为bmol·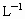 的
的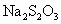 溶液和碘反应,消耗Vml(用淀粉作指示剂).上述过程的反应为:
溶液和碘反应,消耗Vml(用淀粉作指示剂).上述过程的反应为: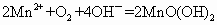
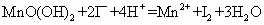
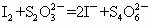
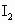 和
和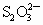 的反应达到反应终点时,溶液颜色变化情况是________.
的反应达到反应终点时,溶液颜色变化情况是________.