题目内容
【题目】25℃时,用0.1000 mol·L-1NaOH溶液分别滴定20.00ml 0.1000 mol·L-1的盐酸和醋酸,滴定曲线如图所示,下列说法正确的是( )
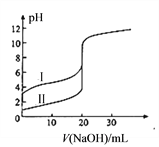
A. Ⅰ、Ⅱ分别表示盐酸和醋酸的滴定曲线
B. pH=7时,滴定盐酸和醋酸消耗NaOH溶液的体积不相等
C. V(NaOH) =10.00mL时,醋酸溶液中:c(Na+)>c(CH3COO-)>c(OH-) >c(H+)
D. V(NaOH) =20.00mL时,两溶液中 c(CH3COO-)>c(Cl-)
【答案】B
【解析】A.根据图示可知,Ⅰ的pH较大,Ⅱ的pH较小,则Ⅰ表示的是醋酸,Ⅱ表示盐酸,故A错误;B.醋酸为弱酸,溶液体积相同时,醋酸和氯化氢的物质的量相等,醋酸与氢氧化钠反应生成醋酸钠,溶液呈碱性,若pH=7时,醋酸的体积应该稍大,故B正确;C.V(NaOH)=10.00mL时,反应后溶质浓度相同的醋酸和醋酸钠,醋酸的电离程度较大,溶液呈酸性,则c(H+)>c(OH-),反应后溶液中离子浓度大小为:c(CH3COO-)>c(Na+)>c(H+)>c(OH-),故C错误;D.V(NaOH)=20.00mL时,两溶液都恰好反应,由于醋酸根离子部分水解,则两溶液中c(CH3COO-)<c(Cl-),故D错误;故选B。

练习册系列答案
相关题目
