题目内容
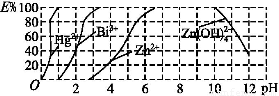
进行污水处理分析时,常用双硫腙(H2Dz,二元弱酸)把金属离子络合成电中性的物质,再用CCl4萃取络合物,从而把金属离子从水溶液中完全分离出来。如用双硫腙(H2Dz)~CCl4分离污水中的Cu2+时,先发生络合反应:Cu2++2H2Dz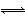 Cu(HDz)2+2H+,再加入CCl4,Cu(HDz)2就很容易被萃取到CCl4中。
Cu(HDz)2+2H+,再加入CCl4,Cu(HDz)2就很容易被萃取到CCl4中。
(1)写出双硫腙和Fe3+络合的离子方程式 ????????????????????????????????????????????????????? ,
萃取Fe3+的过程中要控制适宜的酸度,如果溶液的pH过大,其后果是 。
(2)如图是用双硫腙(H2Dz)~CCl4络合萃取某些金属离子的酸度曲线,它反映了萃取某些金属离子时适宜的pH范围。E%表示某种金属离子以络合物形式萃取分离的百分率。
某工业废水中含有Hg2+、Bi3+、Zn2+,用双硫腙(H2Dz)~CCl4络合萃取法处理废水。
①欲完全将废水中的Hg2+分离出来,须控制溶液的pH= 。
②当调节pH=2时,铋(Bi)的存在形式有 ,其物质的量之比为 。
③萃取到CCl4中的Zn(HDz)2分液后,加入足量NaOH溶液,充分振荡后,锌又转到水溶液中。写出反应的离子方程式: ?????????????????????????????????????????????????????
(3)污水中的亚汞离子(H )必须转换成汞离子(Hg2+)才能用双硫腙络合。某工厂污水中含有较多的氯化亚汞(Hg2Cl2),加入二硫酸钾(K2S2O8)可氧化H
)必须转换成汞离子(Hg2+)才能用双硫腙络合。某工厂污水中含有较多的氯化亚汞(Hg2Cl2),加入二硫酸钾(K2S2O8)可氧化H 生成硫酸汞,写出该反应的化学方程式: 。
生成硫酸汞,写出该反应的化学方程式: 。
(1)F +3H2Dz
+3H2Dz Fe(HDz)3+3H+ Fe3+会形成Fe(OH)3沉淀
Fe(HDz)3+3H+ Fe3+会形成Fe(OH)3沉淀
(2)①1 ②Bi3+、Bi(HDz)3 B ∶Bi(HDz)3=3∶2
∶Bi(HDz)3=3∶2
③Zn(HDz)2+6OH- Zn(OH
Zn(OH +2Dz2-+2H2O
+2Dz2-+2H2O
(3)Hg2Cl2+K2S2O8 2HgSO4+2KCl
2HgSO4+2KCl
【解析】(2)pH=2时Bi萃取分离的百分率40%,有40%的Bi以Bi(HDz)3的形式存在,60%的Bi以Bi3+的形式存在;③由图像可知pH>10时,Zn(HDz)2开始转化为Zn(OH ,H2Dz属于二元弱酸,最终以Dz2-形式存在
,H2Dz属于二元弱酸,最终以Dz2-形式存在

| |||||||||||||||||||||


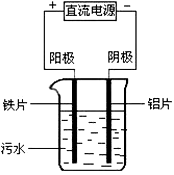
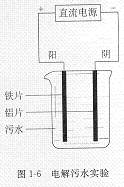 电源正极相连的阳极铁失去电子生成Fe2+,进一步被氧化,并生成Fe(OH)3沉淀,Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化的作用;与直流电源负极相连的阴极产生H2,气泡把污水中悬浮物带到水面形成浮渣层,积累到一定厚度时刮去(或撇掉)浮渣层,即起到了浮选净化的作用。
电源正极相连的阳极铁失去电子生成Fe2+,进一步被氧化,并生成Fe(OH)3沉淀,Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化的作用;与直流电源负极相连的阴极产生H2,气泡把污水中悬浮物带到水面形成浮渣层,积累到一定厚度时刮去(或撇掉)浮渣层,即起到了浮选净化的作用。