题目内容
【题目】氮化锶(Sr3N2)在工业上有广泛的应用,某学习兴趣小组拟设计以下两套实验方案制备氮化锶。已知:锶与氮气在加热条件下反应产生氮化锶,氮化锶遇水剧烈反应产生氢氧化锶和氨气。方案Ⅰ:根据下列装置制备氮化锶。

回答下列问题:
(1)Sr在元素周期表中的位置是____________________
(2)写出A装置中饱和氯化铵溶液和NaNO2溶液反应的化学方程式__________________________
(3)按气流方向,写出装置的连接顺序为___________(装置可重复使用,填字母表示)。
(4)实验时先点燃_____处酒精灯(填“A”或“B”),一段时间后,点燃另一只酒精灯。

方案Ⅱ:某氮气样品可能含有少量的CO、CO2、O2等气体杂质,某同学设计如下装置制备氮化锶(各装置盛装足量试剂)。已知:醋酸二氨合亚铜CH3COO[Cu(NH3)2]溶液能定量吸收CO,但易被O2氧化,失去吸收CO能力;连苯三酚碱性溶液能定量吸收O2。
(5)试管Ⅲ盛装的试剂是_____________________(写试剂的名称)。
(6)测定产品纯度:取Xg产品,向其中加入适量的水。将产生的气体全部通入到浓硫酸中,浓硫酸增重mg,则产品纯度为______(用代数式表示)。
(7)有同学认为上述方法使测得产品纯度偏高,其原因是___________。
【答案】第五周期 ⅡA NH4Cl+NaNO2=N2+NaCl+2H2O ACBC A 醋酸二氨合亚铜 146m/(17X)×100% 氨气中混有水蒸气
【解析】
(1)锶与金属钙位于同一主族,通过分析钙在周期表的位置,推理出锶在周期表中位置;
(2)饱和氯化铵溶液和NaNO2溶液发生归中反应生成氮气,据此写出化学方程式;
(3)由于氮化锶遇水剧烈反应生成氢氧化锶和氨气,所以需要对氨气进行干燥,同时还需要防止空气中的水蒸气和二氧化碳进入硬质玻璃管中,据此进行装置的连接;
(4) 体系内有空气,氧气会和锶反应;实验前先排除装置内氧气;
(5)根据实验目的可知,氮气样品先通过试管I氢氧化钠溶液,除去二氧化碳气体,试管II中加入连苯三酚碱性溶液,能定量吸收O2,试管Ⅲ盛装的试剂是醋酸二氨合亚铜溶液,能定量吸收CO,据此进行分析;
(6) 浓硫酸增重mg为吸收的氨气的质量,根据氮原子守恒,可知氮化锶(Sr3N2)的量和质量,进而计算出产品的纯度;
(7)实验过程造成硫酸质量增加的,都会引起m偏大,使测得产品纯度偏高;据此进行分析。
(1)金属钙的核电荷数为20,在周期表中4周期IIA族,Sr元素与钙元素属于同一主族,且锶位于钙的下一周期,所以Sr在元素周期表中的位置是第五周期 、ⅡA族;
综上所述,本题答案是:第五周期 ⅡA。
(2)根据题目信息可知,饱和氯化铵溶液和NaNO2溶液发生归中反应生成氮气,A装置中的化学方程式:NH4Cl+NaNO2=N2+NaCl+2H2O;
综上所述,本题答案是:NH4Cl+NaNO2=N2+NaCl+2H2O。
(3)由于氮化锶遇水剧烈反应生成氢氧化锶和氨气,所以需要对氨气进行干燥,同时还需要防止空气中的水蒸气和二氧化碳进入硬质玻璃管中,故装置的接口顺序为:ACBC;
综上所述,本题答案是:ACBC。
(4)体系内有空气,氧气会和锶反应;因此实验时先点燃A处酒精灯,反应产生的气体排净装置内的空气,防止锶与氧气反应;
综上所述,本题答案是:A。
(5)根据实验目的可知,氮气样品先通过试管I中的氢氧化钠溶液,除去二氧化碳气体,通过试管II中的连苯三酚碱性溶液,能定量吸收O2,通过试管Ⅲ中的醋酸二氨合亚铜溶液,能定量吸收CO;
综上所述,本题答案是:醋酸二氨合亚铜;
(6) 浓硫酸增重mg为吸收的氨气的质量,根据氮原子守恒,可知氮化锶(Sr3N2)的量为1/2×m/17mol,其质量为292×1/2×m/17g,则产品纯度为[292×1/2×m/17]/ X×100%=146m/(17X)×100% ;
综上所述,本题答案是:146m/(17X)×100% 。
(7)如果氨气中混有水蒸气,造成浓硫酸质量增加的较多,造成m偏大,使测得产品纯度偏高;
综上所述,本题答案是:氨气中混有水蒸气;

【题目】室温时,向试管中通入气体X(如图),下列实验中预测的现象与实际不相符的是
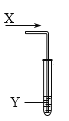
选项 | 气体X | 试管中的物质Y | 预测现象 |
A | 乙烯 | Br2的CCl4溶液 | 溶液橙色逐渐褪去,最终液体分为上下两层 |
B | SO2 | 品红溶液 | 溶液红色逐渐褪去 |
C | 甲烷 | 酸性KMnO4溶液 | 无明显现象,溶液紫色不褪 |
D | 氯气 | FeCl2溶液(浅绿色) | 溶液由浅绿色逐渐变为黄色 |
A. AB. BC. CD. D


