题目内容
含NaOH 20.0g的稀溶液与足量稀盐酸反应,放出28.6kJ的热量,表示该反应中和热的热化学方程式正确的是( )
| A.NaOH(aq)+HCl(aq) = NaCl(aq)+H2O(1)DH=+28.6kJ/mol |
| B.NaOH(aq)+HCL(aq) = NaCl(aq)+H2O(1)DH=-28.6kJ/mol |
| C.NaOH(aq)+HCl(aq) = NaCl(aq)+H2O(1)DH=+57.2kJ/mol |
| D.NaOH(aq)+HCl(aq) = NaCl(aq)+H2O(1)DH=-57.2kJ/mol |
D
正确答案:D
NaOH 20.0g为0.5mol,放出28.6kJ的热量,1mol,放出57.2kJ的热量,D正确。

练习册系列答案
相关题目
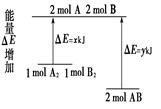
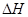 的绝对值均正确)( )
的绝对值均正确)( )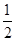 O2(g)=CO2(g) △H= —283kJ/mol
O2(g)=CO2(g) △H= —283kJ/mol H2(g)+CO2(g)△H=
H2(g)+CO2(g)△H= 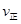 (CO)=
(CO)= (H2O) d.c(CO)=c(H2)
(H2O) d.c(CO)=c(H2) 
 (CO2)表示的反应速率为 。
(CO2)表示的反应速率为 。

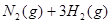

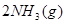 △H=
△H=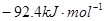 ,恒温、恒容且容积相同的两个密闭容器A、B,A中通入1molN2、3 molH 2,B 中通入0.5 molN2、1.5 mol H 2,反应一段时间后,A、B中均达到平衡状态。下列判断正确的是( )
,恒温、恒容且容积相同的两个密闭容器A、B,A中通入1molN2、3 molH 2,B 中通入0.5 molN2、1.5 mol H 2,反应一段时间后,A、B中均达到平衡状态。下列判断正确的是( )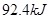
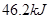
 CO2(g) ΔH=E1 ①
CO2(g) ΔH=E1 ① _____(填“大于”、“等于”、“小于”)途径II放出的热量。
_____(填“大于”、“等于”、“小于”)途径II放出的热量。 是_____________________________________。
是_____________________________________。