题目内容
下列叙述中正确的是
[ ]
A.两种导电能力弱的电解质溶液混合后,所得溶液的导电能力一定更弱
B.向Ba(OH)2溶液中滴加稀H2SO4,溶液的导电能力先变弱后又变强
C.强电解质的溶液中,没有任何分子存在
D.向稀H2SO4溶液中加入少量的NaOH固体,溶液的导电能力几乎不变
答案:BD
解析:
解析:
|
导电性的强弱取决于相同条件下溶液中自由离子的浓度及其所带的电荷.导电性的强弱与电解质的强弱没有必然的联系. 向Ba(OH)2中滴H2SO4,由于发生Ba(OH)2+H2SO4=BaSO4↓+2H2O反应,使溶液中离子浓度减小,导电性相应的减弱.但沉淀完全后继续加H2SO4,则溶液中的离子浓度又增大了,导电性也随之增强. |

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
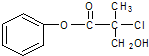 有机物A是农药生产中的一种中间体,结构简式如图所示.下列叙述中正确的是( )
有机物A是农药生产中的一种中间体,结构简式如图所示.下列叙述中正确的是( )| A、有机物A可以在一定条件下与HBr发生反应 | B、1mol A最多能与4mol H2发生加成反应 | C、有机物A与浓硫酸混合加热,可以发生消去反应 | D、1mol A与足量的NaOH溶液反应,最多可以消耗3mol NaOH |


