题目内容
下列有关物质用途的说法中,正确的是
| A.二氧化硅可用作半导体材料 | B.硝酸常用作金属铜加工前的酸洗 |
| C.碳酸钠可用于治疗胃酸过多 | D.三氧化二铁常用于生产红色油漆和涂料 |
D
解析试题分析:A、硅可用作半导体材料,错误;B、硝酸的氧化性较强,可与金属铜反应,放出有刺激性气味的气体,一般用稀盐酸,错误;C、碳酸钠的碱性强于碳酸氢钠,与盐酸反应产生大量二氧化碳气体,影响人体健康,所以一般用小苏打治疗胃酸过多,错误;D、三氧化二铁俗称铁红,常用于生产红色油漆和涂料,正确,答案选D。
考点:考查常见物质的用途

练习册系列答案
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案
相关题目
下列有关NaHCO3与Na2CO3的性质说法中,正确的是
| A.往两者饱和溶液中通入CO2,最终会形成澄清溶液的是NaHCO3 |
| B.除去碳酸氢钠固体中混有的少量碳酸钠可以采用加热的方法 |
| C.碳酸钠与盐酸反应放出二氧化碳的剧烈程度强于碳酸氢钠 |
| D.二者配成溶液,再加入石灰水,无白色沉淀生成的是NaHCO3 |
某化学小组为测定一定质量的某铜铝混合物中铜的质量分数,设计了如下实验方案:
方案Ⅰ:铜铝混合物 测定生成气体的体积
测定生成气体的体积
方案Ⅱ:铜铝混合物 测定剩余固体的质量
测定剩余固体的质量
下列有关判断中不正确的是( )。
| A.溶液A和B均可以是盐酸 |
| B.溶液A和B均可以是NaOH溶液 |
| C.溶液A和B均可选用稀硝酸 |
| D.实验室中方案Ⅱ更便于实施 |
下列类比关系正确的是 ( )。
| A.AlCl3与过量NaOH溶液反应生成AlO2-,则与过量NH3·H2O也生成AlO2- |
| B.Na2O2与CO2反应生成Na2CO3和O2,则与SO2反应可生成Na2SO3和O2 |
| C.Fe与Cl2反应生成FeCl3,则与I2反应可生成FeI3 |
| D.Al与Fe2O3能发生铝热反应,则与MnO2也能发生铝热反应 |
下列氧化物不能跟铝粉组成铝热剂的是( )。
| A.Cr2O3 | B.MnO2 | C.MgO | D.V2O5 |
海水是镁的主要来源之一,从海水中提取镁可按如下步骤进行:①把贝壳(主要成分是碳酸钙)煅烧成石灰;②在引有海水的渠中加入石灰,经过沉降,然后过滤得沉淀物;③将沉淀物与稀盐酸反应,然后结晶、过滤、干燥;④电解得产品。以上提取镁的全过程中,没有涉及的反应类型有( )
| A.分解反应 | B.化合反应 |
| C.置换反应 | D.复分解反应 |
下列叙述中,正确的是( )
| A.氯化铝溶液中加入过量氨水反应实质是: Al3++3NH3·H2O=Al(OH)3↓+3NH4+ |
| B.在加入铝粉能放出氢气的溶液中:K+、NH4+、CO32—、Cl-一定能够大量共存 |
| C.镁铝合金既可完全溶于过量盐酸又可完全溶于过量NaOH溶液 |
D.依据铝热反应原理,能发生反应:2Al+3MgO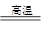 3Mg+Al2O3 3Mg+Al2O3 |
FeCl3、CuCl2的混合溶液中加入铁粉,充分反应后仍有固体存在,则下列判断不正确的是( )
| A.加入KSCN溶液一定不变红色 |
| B.溶液中一定含Fe2+ |
| C.溶液中一定含Cu2+ |
| D.剩余固体中一定含Cu |
用黄色的FeCl3溶液分别进行下列实验,解释或结论不正确的是( )
| 选项 | 实验 | 现象 | 解释或结论 |
| A | 加入FeCl3固体 | 溶液变成红褐色 | FeCl3的水解程度变大 |
| B | 加入等体积水 | 溶液颜色变浅 | c(Fe3+)变小 |
| C | 加入足量Fe粉 | 溶液颜色变成浅绿色 | 2Fe3++Fe=3Fe2+ |
| D | 将FeCl3溶液微热 | 溶液变成红褐色 | 水解反应 ΔH>0 |