题目内容
标准状况下,将5.6L由CO、CH4、C2H4、C2H2组成的混合气体与18L O2混合于某密闭容器中点燃,反应完成后再恢复到原状况,得CO2气体7.50L,则下列判断中正确的是
| A.反应完成后,O2剩余 |
| B.原混合气体中,C2H4和C2H2的体积共为1.9L |
| C.反应完全后,生成水的质量为9g |
| D.原混合气体中,CO与CH4的体积比一定为1:1 |
AB
A:由各气体的完全燃烧方程式可知,各气体与氧气的体积比分别为2:1、1:2、1:3、1:2.5,即使气体全部是乙烯,5.6L气体也最多需要氧气体16.8L,故氧气有剩余,正确
B:CO、CH4均含有一个碳原子,与各自燃烧生成的CO2的体积相当,而C2H4、C2H2均含有两个碳原子,与与各自燃烧生成的CO2的体积比为1:2,故混合气体体积的增加值即就是C2H4、C2H2的总体积,也就是1.9升,正确
CD无法计算确定,排除
答案为AB
B:CO、CH4均含有一个碳原子,与各自燃烧生成的CO2的体积相当,而C2H4、C2H2均含有两个碳原子,与与各自燃烧生成的CO2的体积比为1:2,故混合气体体积的增加值即就是C2H4、C2H2的总体积,也就是1.9升,正确
CD无法计算确定,排除
答案为AB

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
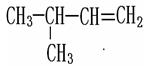 ⑺红磷 ⑻3717Cl
⑺红磷 ⑻3717Cl