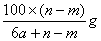题目内容
某温度时,用惰性电极电解硝酸钠的不饱和溶液.若两极板收集到气体总体积为22.4aL时,剩余溶液恢复至原温度,析出溶质mg(溶质不带结晶水);若两极收集到气体总体积为33.6aL时,剩余溶液恢复至原温度,析出溶质ng.则硝酸钠在该温度时的溶解度是(气体体积均已折合为标准状况下的体积)( )A.
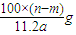
B.
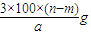
C.
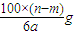
D.
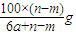
【答案】分析:依据电解原理分析.用惰性电极电解硝酸钠溶液实质是电解水,依据电解产生的气体是阳极为氧气,阴极为氢气,在两次电解后都析出晶体,所以两次电解水的差值得到的水的质量和两次析出晶体的差值溶质的质量,是饱和溶液的组成,依据溶解度的概念是一定温度下,100克水中达到饱和时溶解溶质的质量称为溶解度分析计算;
解答:解:用惰性电极电解硝酸钠的不饱和溶液.若两极板收集到气体总体积为22.4aL时,阳极反应生成氧气,阴极生成氢气,水中是电解水,氧气和氢气物质的量之比为1:2,所以22.4aL气体物质的量为amol,其中氧气 amol,氢气
amol,氢气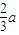 mol,电解水物质的量为
mol,电解水物质的量为 amol;同样若两极收集到气体总体积为33.6aL时,气体为氧气和氢气混合物物质的量为1.5amol,其中氧气
amol;同样若两极收集到气体总体积为33.6aL时,气体为氧气和氢气混合物物质的量为1.5amol,其中氧气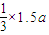 =0.5amol,氢气为
=0.5amol,氢气为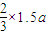 =amol,电解水物质的量为amol;第一次析出溶质mg,第二次剩余溶液恢复至原温度,析出溶质ng,实质是(n-m)g晶体溶解在两次电解水的质量差中会形成饱和溶液,两次电解的水物质的量的差值为amol-
=amol,电解水物质的量为amol;第一次析出溶质mg,第二次剩余溶液恢复至原温度,析出溶质ng,实质是(n-m)g晶体溶解在两次电解水的质量差中会形成饱和溶液,两次电解的水物质的量的差值为amol- amol=
amol= amol,质量为=
amol,质量为=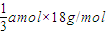 =6ag,即6ag水溶解(n-m)g晶体形成饱和吸收钠溶液,根据溶解度S的概念计算:6a:(n-m)=100:S,S=
=6ag,即6ag水溶解(n-m)g晶体形成饱和吸收钠溶液,根据溶解度S的概念计算:6a:(n-m)=100:S,S=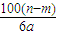 g;
g;
故选C.
点评:本题考查了电解原理的过程和电解反应的计算,溶解度概念的应用,关键是两次电解水的差值和析出晶体的差值混合为饱和溶液的应用.
解答:解:用惰性电极电解硝酸钠的不饱和溶液.若两极板收集到气体总体积为22.4aL时,阳极反应生成氧气,阴极生成氢气,水中是电解水,氧气和氢气物质的量之比为1:2,所以22.4aL气体物质的量为amol,其中氧气
 amol,氢气
amol,氢气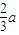 mol,电解水物质的量为
mol,电解水物质的量为 amol;同样若两极收集到气体总体积为33.6aL时,气体为氧气和氢气混合物物质的量为1.5amol,其中氧气
amol;同样若两极收集到气体总体积为33.6aL时,气体为氧气和氢气混合物物质的量为1.5amol,其中氧气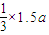 =0.5amol,氢气为
=0.5amol,氢气为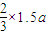 =amol,电解水物质的量为amol;第一次析出溶质mg,第二次剩余溶液恢复至原温度,析出溶质ng,实质是(n-m)g晶体溶解在两次电解水的质量差中会形成饱和溶液,两次电解的水物质的量的差值为amol-
=amol,电解水物质的量为amol;第一次析出溶质mg,第二次剩余溶液恢复至原温度,析出溶质ng,实质是(n-m)g晶体溶解在两次电解水的质量差中会形成饱和溶液,两次电解的水物质的量的差值为amol- amol=
amol= amol,质量为=
amol,质量为=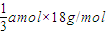 =6ag,即6ag水溶解(n-m)g晶体形成饱和吸收钠溶液,根据溶解度S的概念计算:6a:(n-m)=100:S,S=
=6ag,即6ag水溶解(n-m)g晶体形成饱和吸收钠溶液,根据溶解度S的概念计算:6a:(n-m)=100:S,S=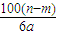 g;
g;故选C.
点评:本题考查了电解原理的过程和电解反应的计算,溶解度概念的应用,关键是两次电解水的差值和析出晶体的差值混合为饱和溶液的应用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
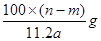 B.
B.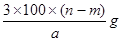
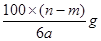 D.
D.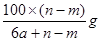
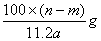 B、
B、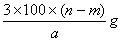
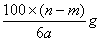 D、
D、