题目内容
(08年龙海五中最后三卷)下面是有关物质的转化关系图(有些物质己省略),其中A为单质,E常温下为液体,D是一种含氧的化合物,请回答相关问题 。
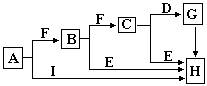
(1)若C的式量为78,则对C的结构、性质推断中不正确的是__________。
A.久置于空气中会变成白色 B.具有强的氧化性
C.晶体存在离子键与非极性键
D.与湿润的紫色石蕊试纸接触时,只能使试纸变蓝色
(2)A的原子结构简图___________,H的电子式__________。
E的结构式____________。
(3)若C也是含氧化合物且氧为18O时,写出C与D反应的方程式:________。
另一产物(D以外)的摩尔质量为__________。
(4)当A量较少时,I不可能是_____________。
A.H2O B.NaCl(aq) C.NaOH(aq) D.CuCl2
(5)若没有E在常温下为无色液体的限制,则E、I还可分别是:__________,_______(填物质名称)
答案:(1) D(2分) (2)![]() 、
、![]() H-O-H或
H-O-H或![]() (3分)
(3分)
(3)2Na218O2+2CO2=2Na2CO2?18O+ 18O2、36g/mol,(3分)
(4)D (2分) (5)盐酸或SO3、氯气或硫酸(2分)
解析:单质A能与同一物质F连续发生两次反应,这样的单质常见的有C、S、N2(此时F为O2)或A为P而F为Cl2,结合C的式量值可初步确定A为钠、C为Na2O2、B为Na2O、D为CO2、G为Na2CO3、H是NaOH,此时I不可能是CuCl2。Na2O2在空气中会与CO2反应最终转化为Na2CO3白色固体,晶体中存在钠氧离子键与“O-O”共价键,其中的氧元素为-1价,具有强的氧化性,能漂白包括酸碱指示剂在内的许多有色物质;也能表现出一定的还原性;与水或CO2反应是一个自身氧化还原反应。当E为盐酸或SO3、I为氯气或硫酸时也能实现上述变化。

 中考解读考点精练系列答案
中考解读考点精练系列答案
 (08年龙海五中最后三卷)氢能是理想的无污染的绿色能源,利用太阳能光催化裂解水制取氢气是能源的一次新技术革命。钙钛矿型层状氧化物是一种新型光催化剂。右图为钙铁矿晶体结构示意圈.下列有关说法不正确的是( )
(08年龙海五中最后三卷)氢能是理想的无污染的绿色能源,利用太阳能光催化裂解水制取氢气是能源的一次新技术革命。钙钛矿型层状氧化物是一种新型光催化剂。右图为钙铁矿晶体结构示意圈.下列有关说法不正确的是( )