题目内容
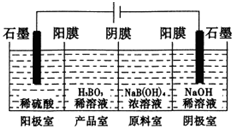
16. 元素周期表中钠元素的信息如图所示,对图中信息理解不正确的是( )
元素周期表中钠元素的信息如图所示,对图中信息理解不正确的是( )| A. | 质子数为11 | B. | 元素名称为钠 | ||
| C. | 元素符号为 Na | D. | 核外电子数为22.99 |
分析 根据图中元素周期表可以获得的信息:原子序数、相对原子质量、元素符号、元素种类等,进行分析判断即可.
解答 解:A、根据元素周期表中的一格中获取的信息,该元素的原子序数为11;由原子序数=核电荷数=质子数=核外电子数,则该元素的原子核内质子数为11,故A正确;
B、根据元素周期表中的一格中获取的信息,该元素的元素名称是钠,故B正确;
C、根据元素周期表中的一格中获取的信息,该元素的元素符号是Na,故C正确;
D、根据元素周期表中的一格中获取的信息,可知该元素的相对原子质量为22.99;由原子序数=核电荷数=质子数=核外电子数,则该元素的原子核外电子数应为11,故D错误;
故选D.
点评 本题难度不大,考查学生对元素周期表中一格信息的理解,掌握并能灵活运用元素周期表中元素的信息是正确解答此类题的关键.

练习册系列答案
相关题目
6.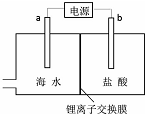 海水中含有丰富的锂资源,研究人员开发了一种只能让锂离子通过的特殊交换膜,并运用电解实现从海水中提取高浓度的锂盐,其工作原理如图所示?下列说法不正确的是( )
海水中含有丰富的锂资源,研究人员开发了一种只能让锂离子通过的特殊交换膜,并运用电解实现从海水中提取高浓度的锂盐,其工作原理如图所示?下列说法不正确的是( )
 海水中含有丰富的锂资源,研究人员开发了一种只能让锂离子通过的特殊交换膜,并运用电解实现从海水中提取高浓度的锂盐,其工作原理如图所示?下列说法不正确的是( )
海水中含有丰富的锂资源,研究人员开发了一种只能让锂离子通过的特殊交换膜,并运用电解实现从海水中提取高浓度的锂盐,其工作原理如图所示?下列说法不正确的是( )| A. | a连接电源的正极 | |
| B. | Li+的移动方向是从海水进入到盐酸中 | |
| C. | 一段时间后,b电极附近溶液的pH降低 | |
| D. | 电解过程中还可能获得有经济价值的副产物氢气和氯气 |
7.其他条件不变,升高温度下列数据一定增大的是( )
| A. | 碱在水中的溶解度 | B. | 乙酸溶液的pH | ||
| C. | 合成氨的反应热 | D. | 醋酸钠溶液中的氢氧根离子浓度 |
4.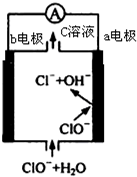 镁-次氯酸盐燃料电池的工作原理如图,该电池反应为:Mg+ClO -+H2O═Mg(OH)2+Cl-下列有关说法正确的是( )
镁-次氯酸盐燃料电池的工作原理如图,该电池反应为:Mg+ClO -+H2O═Mg(OH)2+Cl-下列有关说法正确的是( )
 镁-次氯酸盐燃料电池的工作原理如图,该电池反应为:Mg+ClO -+H2O═Mg(OH)2+Cl-下列有关说法正确的是( )
镁-次氯酸盐燃料电池的工作原理如图,该电池反应为:Mg+ClO -+H2O═Mg(OH)2+Cl-下列有关说法正确的是( )| A. | 电池工作时,C溶液中的溶质是MgCl2 | |
| B. | 电池工作时,正极a附近的PH将不断增大 | |
| C. | 负极反应式:ClO --2e -+H2O═Cl-+2 OH- | |
| D. | b电极发生还原反应,每转移0.1mol电子,理论上生成0.1mol Cl- |
11.下列日常生活用品不能与水形成溶液的是( )
| A. | 食盐 | B. | 蔗糖 | C. | 白醋 | D. | 面粉 |
8.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 含大量Fe3+的溶液中:Na+、Mg2+、SO42-、SCN- | |
| B. | $\frac{c(O{H}^{-})}{c({H}^{+})}$=106的溶液中:NH4+、K+、AlO2-、NO3- | |
| C. | 能使甲基橙变红的溶液中:Cu2+、Mg2+、SO42-、Cl- | |
| D. | 1.0 mol•L-1的KNO3溶液中:Fe2+、H+、Cl-、I- |
5.某研究性小组探究乙酸乙酯的反应机理,相关物理性质(常温常压)及仪器如下:
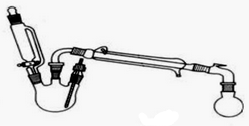
已知:当乙酸乙酯安装物质的量1:1投料时,乙酸的转化率为65%,当乙酸和乙醇按照物质的量1:10投料时,乙酸的转化率为97%(数据均在120℃下测定).
实验过程:
Ⅰ.合成反应:在三颈烧瓶中加入乙醇5mL,浓硫酸5mL,2小片碎瓷片.漏斗加入乙酸14.3 mL,乙醇20 mL.冷凝管中通入冷却水后,开始缓慢加热,控制滴加速度等于蒸馏速度,反应温度不超过120℃.
Ⅱ.分离提纯:将反应粗产物倒入分液漏斗中,依次用少量饱和的Na2CO3溶液、饱和NaCl溶液、饱和CaCl2溶液洗涤,分离后加入无水碳酸钾,静置一段时间后弃去碳酸钾.最终通过蒸馏得到纯净的乙酸乙酯.
回答下列问题:
(1)酯化反应的机理探究
A、乙醇羟基氧示踪
CH2CO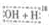 OCH2CH3$?_{△}^{浓硫酸}$CH3CO18OCH2CH3+H2O
OCH2CH3$?_{△}^{浓硫酸}$CH3CO18OCH2CH3+H2O
B、用醋酸烃基氧示踪

实验B发现,产物中含氧-18水占到总水量的一半,酯也一样.这个实验推翻了酯化反应为简单的取代反应的结论.请你设想酯化反应的机理先加成反应生成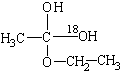 后消去失水,失水有两种可能分别生成
后消去失水,失水有两种可能分别生成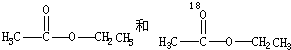 .
.
(2)酯化反应是一个可逆的反应,120℃时,平衡常数K=3.45.
(3)如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是B(填正确答案标号).
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(4)本实验用到的量取液体体积的仪器是量筒,浓硫酸与乙醇混合应怎样操作?先加入乙醇后加入硫酸,边振荡加滴加.
(5)控制滴加乙酸和乙醇混和液的速度等于蒸馏速度目的是保证乙醇量是乙酸量10倍以上,提高乙酸的转化率.
(6)蒸出的粗乙酸乙酯中主要有哪些杂质乙醚、乙酸、乙醇和水.用饱和NaCl溶液洗涤除去残留的Na2CO3溶液,为什么不用水?减少乙酸乙酯溶解.
| 密度g/mL | 熔点/℃ | 沸点/℃ | 水溶性 | |
| 乙醇 | 0.79 | -114 | 78 | 溶 |
| 乙酸 | 1.049 | 16.2 | 117 | 溶 |
| 乙酸乙酯 | 0.902 | -84 | 76.5 | 不溶 |

已知:当乙酸乙酯安装物质的量1:1投料时,乙酸的转化率为65%,当乙酸和乙醇按照物质的量1:10投料时,乙酸的转化率为97%(数据均在120℃下测定).
实验过程:
Ⅰ.合成反应:在三颈烧瓶中加入乙醇5mL,浓硫酸5mL,2小片碎瓷片.漏斗加入乙酸14.3 mL,乙醇20 mL.冷凝管中通入冷却水后,开始缓慢加热,控制滴加速度等于蒸馏速度,反应温度不超过120℃.
Ⅱ.分离提纯:将反应粗产物倒入分液漏斗中,依次用少量饱和的Na2CO3溶液、饱和NaCl溶液、饱和CaCl2溶液洗涤,分离后加入无水碳酸钾,静置一段时间后弃去碳酸钾.最终通过蒸馏得到纯净的乙酸乙酯.
回答下列问题:
(1)酯化反应的机理探究
A、乙醇羟基氧示踪
CH2CO
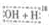 OCH2CH3$?_{△}^{浓硫酸}$CH3CO18OCH2CH3+H2O
OCH2CH3$?_{△}^{浓硫酸}$CH3CO18OCH2CH3+H2OB、用醋酸烃基氧示踪

实验B发现,产物中含氧-18水占到总水量的一半,酯也一样.这个实验推翻了酯化反应为简单的取代反应的结论.请你设想酯化反应的机理先加成反应生成
 后消去失水,失水有两种可能分别生成
后消去失水,失水有两种可能分别生成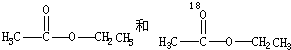 .
.(2)酯化反应是一个可逆的反应,120℃时,平衡常数K=3.45.
(3)如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是B(填正确答案标号).
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(4)本实验用到的量取液体体积的仪器是量筒,浓硫酸与乙醇混合应怎样操作?先加入乙醇后加入硫酸,边振荡加滴加.
(5)控制滴加乙酸和乙醇混和液的速度等于蒸馏速度目的是保证乙醇量是乙酸量10倍以上,提高乙酸的转化率.
(6)蒸出的粗乙酸乙酯中主要有哪些杂质乙醚、乙酸、乙醇和水.用饱和NaCl溶液洗涤除去残留的Na2CO3溶液,为什么不用水?减少乙酸乙酯溶解.