题目内容
 某学生利用物质间的互变,设计成一个平面魔方,如图所示:
某学生利用物质间的互变,设计成一个平面魔方,如图所示:
已知:
①A、B、C、D、G含有同种元素.
②E是通常情况下密度最小的气体;B与硝酸银溶液反应生成不溶于稀硝酸的白色沉淀.B具有氧化性,液显黄色,能将SO2氧化为F(H2SO4),F与A反应生成E、G.
③
| 纯A(单质) | B溶液 | C固体 | D固体 | G溶液 | |
| 颜色 | 银白色 | 黄色 | 红褐色 | 红棕色 | 浅绿色 |
(1)请写出E的电子式______、D的化学式______.
(2)请指出A、B、C、D、G所含的同种元素在周期表中的位置第______周期,第______族
(3)G生成C的过程中所出现的现象为______
(4)写出下列反应的化学方程式:
E→A______
A→B______
(5)B→F的离子方程式为______.
解:(1)E是通常情况下密度最小的气体,E是氢气,B与硝酸银溶液反应生成不溶于稀硝酸的白色沉淀,说明B中有氯元素,B溶液显黄色,又知B具有氧化性,能将SO2氧化为硫酸,则B是FeCl3,C固体是红褐色,为Fe(OH)3,根据图示,D为Fe2O3,则A、B、C、D、G含有同种元素为铁元素,硫酸与铁反应生成E、G,G溶液为浅绿色,所以G为FeSO4,E是H2,
故答案为:H:H;Fe2O3;
(2)铁的原子序数为26,根据原子序数和原子核外电子排布可知铁在元素周期表中第四周期、第Ⅷ族,故答案为:四;Ⅷ;
(3)G为硫酸亚铁,加入碱生成白色的氢氧化亚铁,氢氧化亚铁不稳定,易与氧气反应生成红褐色的氢氧化铁沉淀,故答案为:先产生白色沉淀,逐渐变为灰绿色,最后变为红褐色;
(4)氢气具有还原性,在加热条件下与四氧化三铁反应生成单质铁;铁与强氧化剂氯气反应生成最高价态的氯化铁,故答案为:4H2+Fe3O4 3Fe+4H2O;2Fe+3Cl2
3Fe+4H2O;2Fe+3Cl2  2FeCl3;
2FeCl3;
(5)Fe3+具有氧化性,SO2具有还原性,二者发生氧化还原反应生成Fe2++和SO42-离子,
故答案为:2Fe3++SO2+2H2O═2Fe2++SO42-+4H+.
分析:E是通常情况下密度最小的气体,E是氢气,B与硝酸银溶液反应生成不溶于稀硝酸的白色沉淀,说明B中有氯元素,B溶液显黄色,又知B具有氧化性,能将SO2氧化为硫酸,则B是FeCl3,C固体是红褐色,为Fe(OH)3,根据图示,D为Fe2O3,则A、B、C、D、G含有同种元素为铁元素,硫酸与铁反应生成E、G,G溶液为浅绿色,所以G为FeSO4,E是H2,以此来回答在周期表中的位置、化学式、反应现象等问题.
点评:本题考查属于物质的推断题目,考查电子式的书写,周期表中的位置、物质的性质,本题的突破口在于一些物质的特殊性质,在学习中要注意积累.
故答案为:H:H;Fe2O3;
(2)铁的原子序数为26,根据原子序数和原子核外电子排布可知铁在元素周期表中第四周期、第Ⅷ族,故答案为:四;Ⅷ;
(3)G为硫酸亚铁,加入碱生成白色的氢氧化亚铁,氢氧化亚铁不稳定,易与氧气反应生成红褐色的氢氧化铁沉淀,故答案为:先产生白色沉淀,逐渐变为灰绿色,最后变为红褐色;
(4)氢气具有还原性,在加热条件下与四氧化三铁反应生成单质铁;铁与强氧化剂氯气反应生成最高价态的氯化铁,故答案为:4H2+Fe3O4
 3Fe+4H2O;2Fe+3Cl2
3Fe+4H2O;2Fe+3Cl2  2FeCl3;
2FeCl3;(5)Fe3+具有氧化性,SO2具有还原性,二者发生氧化还原反应生成Fe2++和SO42-离子,
故答案为:2Fe3++SO2+2H2O═2Fe2++SO42-+4H+.
分析:E是通常情况下密度最小的气体,E是氢气,B与硝酸银溶液反应生成不溶于稀硝酸的白色沉淀,说明B中有氯元素,B溶液显黄色,又知B具有氧化性,能将SO2氧化为硫酸,则B是FeCl3,C固体是红褐色,为Fe(OH)3,根据图示,D为Fe2O3,则A、B、C、D、G含有同种元素为铁元素,硫酸与铁反应生成E、G,G溶液为浅绿色,所以G为FeSO4,E是H2,以此来回答在周期表中的位置、化学式、反应现象等问题.
点评:本题考查属于物质的推断题目,考查电子式的书写,周期表中的位置、物质的性质,本题的突破口在于一些物质的特殊性质,在学习中要注意积累.

练习册系列答案
 学习实践园地系列答案
学习实践园地系列答案
相关题目
某学生利用物质间的互变,设计成一个平面魔方,如下图所示:
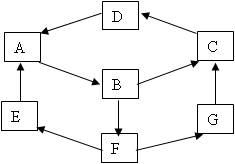
已知①A、B、C、D、G含有同种元素。
②E是通常情况下密度最小的气体;B与硝酸银溶液反应生成不溶于稀硝酸的白色沉淀。B具有氧化性,能将SO2氧化为F(H2SO4),F与A反应生成E、G。
| 纯A(单质) | B溶液 | C固体 | D固体 | G溶液 | |
| 颜色 | 银白色 | 黄色 | 红褐色 | 红棕色 | 浅绿色 |
③
依据以上信息填空:
(1)请写出E的电子式 、D的化学式 。
(2) 请指出A、B、C、D、G所含的同种元素在周期表中的位置第 周期 第 族,
(3)G生成C的过程中所出现的现象为
(4)写出下列反应的化学方程式:
E→A A→B
(5)B→F的离子方程式为
某学生利用物质间的互变,设计成一个平面魔方,如图所示:
已知:
①A、B、C、D、G含有同种元素.
②E是通常情况下密度最小的气体;B与硝酸银溶液反应生成不溶于稀硝酸的白色沉淀.B具有氧化性,液显黄色,能将SO2氧化为F(H2SO4),F与A反应生成E、G.
③
依据以上信息填空:
(1)请写出E的电子式______、D的化学式______.
(2)请指出A、B、C、D、G所含的同种元素在周期表中的位置第______周期,第______族
(3)G生成C的过程中所出现的现象为______
(4)写出下列反应的化学方程式:
E→A______ 3Fe+4H2O

已知:
①A、B、C、D、G含有同种元素.
②E是通常情况下密度最小的气体;B与硝酸银溶液反应生成不溶于稀硝酸的白色沉淀.B具有氧化性,液显黄色,能将SO2氧化为F(H2SO4),F与A反应生成E、G.
③
| 纯A(单质) | B溶液 | C固体 | D固体 | G溶液 | |
| 颜色 | 银白色 | 黄色 | 红褐色 | 红棕色 | 浅绿色 |
(1)请写出E的电子式______、D的化学式______.
(2)请指出A、B、C、D、G所含的同种元素在周期表中的位置第______周期,第______族
(3)G生成C的过程中所出现的现象为______
(4)写出下列反应的化学方程式:
E→A______ 3Fe+4H2O

 某学生利用物质间的互变,设计成一个平面魔方,如图所示:
某学生利用物质间的互变,设计成一个平面魔方,如图所示: