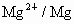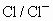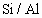题目内容
下列粒子半径之比大于1的是( )
A.r(K+)/r(K) B.r (Ca)/r(Mg)
C.r (P)/r(S) D.r (Cl)/r(Cl-)
答案:BC
提示:
提示:
原子半径的大小主要由核外电子层数和原子核对核外电子的作用两方面因素决定,一般来说,电子层数越多的原子,其半径越大;反之电子层数越少的原子半径越小。当电子层数相同时,随着核电荷数增加,原子半径逐渐减小。由此可判断r(Ca)>r(Mg)>r(P)>r(S)。对同一种元素来说,原子半径>阳离子半径,原子半径<阴离子半径据此可判断r(K+)<r(K),r(Cl)<(Cl-)。故本题答案B、C项。结合物理学知识和化学知识总结的上述规律,很容易理解和记忆,而掌握了这些规律,也就找到了解决比较粒子半径的方法。
|

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目