题目内容
已知:A、B为单质,C为化合物, 。能实现该转化关系的是( )
。能实现该转化关系的是( )
①若C溶于水后得到强碱性溶液,则A可能是Na
②若C的溶液遇Na2CO3放出CO2气体,则A可能是H2
③若C的溶液中滴加KSCN溶液显红色,则B可能为Fe
④若C的溶液中滴加NaOH溶液有蓝色沉淀生成,则B可能为Cu
A.①② B.②④ C.①③ D.③④
B
解析

练习册系列答案
 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案
相关题目
下列实验现象描述正确的是
| A.HCl与NH3相遇有大量的白烟生成 |
| B.用洁净玻棒蘸取Na2SO4溶液灼烧火焰呈紫色 |
| C.FeCl2溶液与无色的KSCN溶液混合,溶液呈红色 |
| D.SO2通入品红溶液,红色褪去,再加热,红色不再出现 |
甲、乙、丙、丁是中学常见的物质,其中甲、乙、丙均含有同一种元素,在一定条件下的转化关系如图,下列说法正确的是
| A.若丁为用量最大,用途最广的金属单质,乙的溶液一定为FeCl3 |
B.若通常情况下甲、乙、丙、丁都是气体,且乙和丁为空气的主要成分,则反应①的化学方程式4NH3+5O2 4NO+6H2O 4NO+6H2O |
| C.若甲、乙、丙的溶液显碱性,丙可作为医疗上治疗胃酸过多症的药剂,将等物质的量的乙和丙溶于水形成混合溶液,溶液中各离子浓度由大到小的顺序为c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)> c(H+) |
| D.若丁为化合物,且为氯碱工业的重要产品,则甲一定为含Al3+的盐 |
下列说法正确的是
| A.实验室常用无水硫酸铜作气体干燥剂 |
| B.工业上常用电解AlCl3,制备金属Al |
| C.CO2溶于水能导电,故CO2是电解质 |
D.NH4C1溶液中离子浓度大小关系为c(Cl-))>(NH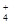 )>c(H+)>c(OH-) )>c(H+)>c(OH-) |
不能证明下列物质具有漂白性的是( )
| A.品红溶液通入SO2后,红色消失 |
| B.显红色的酚酞溶液通入SO2后,红色褪去 |
| C.加有酚酞的水中投入Na2O2粉末溶液先变红,后褪色 |
| D.将新制氯水滴入紫色石蕊试液先变红,后褪色 |
X、Y、Z、W四种短周期元素。X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为17。其中W的阴离子核外电子数与Z原子的最内层电子数相同。X的一种核素在考古时常用来鉴定一些文物的年代,工业上采用液态空气分馏方法来生产Y的单质,而Y、Z均能形成双原子分子。根据以上叙述,下列说法中正确的是
| A.以上四种元素的原子半径大小为X<Y<Z<W |
| B.X2W2、W2Y、WZ均为直线型的共价化合物 |
| C.W与Y形成的化合物W2Y2在化学反应中既可作氧化剂也可作还原剂 |
| D.由W与X组成的化合物的沸点总低于由W与Y组成的化合物的沸点 |
在试管中注入某红色溶液,给试管加热,溶液颜色逐渐变浅,则原溶液可能是( )
①滴有石蕊的H2SO4溶液 ②滴有酚酞的氨水溶液
③滴有酚酞的氢氧化钠溶液 ④滴有酚酞的饱和氢氧化钙溶液 ⑤滴有酚酞的Na2CO3溶液 ⑥溶有SO2的品红溶液
| A.②⑥ | B.②④ | C.①③⑤ | D.②④⑥ |
下列实验的现象与对应结论均正确的是( )
| 选项 | 操作 | 现象 | 结论 |
| A | 将浓硫酸滴到蔗糖表面 | 固体变黑膨胀 | 浓硫酸有脱水性和强氧化性 |
| B | 常温下将Al片放入浓硝酸中 | 无明显现象 | Al与浓硝酸不反应 |
| C | 将一小块Na放入无水乙醇中 | 产生气泡 | Na能置换出醇羟基中的氢 |
| D | 将水蒸气通过灼热的铁粉 | 粉末变红 | 铁与水在高温下发生反应 |