题目内容
下列反应中必须加入还原剂才能进行的是
- A.CuO→CuCl2
- B.Zn→Zn2+
- C.H2→H2O
- D.Fe3+→Fe2+
D
分析:必须加入还原剂才能进行,则选项中发生氧化剂的反应,氧化剂中某元素的化合价降低,以此来解答.
解答:A.CuO→CuCl2中,元素的化合价不变,与盐酸发生非氧化还原反应即可,故A不选;
B.Zn→Zn2+中,Zn元素的化合价升高,则需加氧化剂实现反应,故B不选;
C.H2→H2O中,H元素的化合价升高,则需加氧化剂实现反应,故C不选;
D.Fe3+→Fe2+中,Fe元素的化合价降低,则需要加还原剂实现,故D选;
故选D.
点评:本题考查氧化还原反应,明确氧化剂中某元素的化合价降低及常见的化学反应即可解答,题目难度不大.
分析:必须加入还原剂才能进行,则选项中发生氧化剂的反应,氧化剂中某元素的化合价降低,以此来解答.
解答:A.CuO→CuCl2中,元素的化合价不变,与盐酸发生非氧化还原反应即可,故A不选;
B.Zn→Zn2+中,Zn元素的化合价升高,则需加氧化剂实现反应,故B不选;
C.H2→H2O中,H元素的化合价升高,则需加氧化剂实现反应,故C不选;
D.Fe3+→Fe2+中,Fe元素的化合价降低,则需要加还原剂实现,故D选;
故选D.
点评:本题考查氧化还原反应,明确氧化剂中某元素的化合价降低及常见的化学反应即可解答,题目难度不大.

练习册系列答案
相关题目
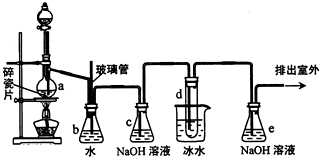 1,2一二溴乙烷可作抗爆剂的添加剂.如图为实验室制备1,2一二溴乙烷的装置图,图中分液漏斗和烧瓶a中分别装有浓H2SO4和无水乙醇,试管d中装有液溴.
1,2一二溴乙烷可作抗爆剂的添加剂.如图为实验室制备1,2一二溴乙烷的装置图,图中分液漏斗和烧瓶a中分别装有浓H2SO4和无水乙醇,试管d中装有液溴.已知:CH3CH2OH
| 浓硫酸 |
| 170℃ |
CH3CH2OH
| 浓硫酸 |
| 140℃ |
相关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | 溴 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 | 红棕色液体 |
| 密度/g.cm-3 | 0.79 | 2.18 | 0.71 | 3.10 |
| 沸点/℃ | 78.5 | 131.4 | 34.6 | 58.8 |
| 熔点/℃ | -114.3 | 9.79 | -116.2 | -7.2 |
| 水溶性 | 混溶 | 难溶 | 微溶 | 可溶 |
(2)安全瓶b在实验中有多重作用.其一可以检查实验进行中导管d是否发生堵塞,请写出发生堵塞时瓶b中的现象;如果实验中导管d堵塞,你认为可能的原因是;安全瓶b还可以起到的作用是
(3)容器c、e中都盛有NaOH溶液,c中NaOH溶液的作用是
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超过许多,如果装置的气密性没有问题,试分析可能的原因
(5)除去产物中少量未反应的Br2后,还含有的主要杂质为
(6)实验中也可以撤去d装置中盛冰水的烧杯,改为将冷水直接加入到d装置的试管内,则此时冷水除了能起到冷却1,2一二溴乙烷的作用外,还可以起到的作用是
 实验室制取溴苯的装置示意图及有关数据如下:
实验室制取溴苯的装置示意图及有关数据如下: (2013?无锡一模)溴苯是一种化工原料,实验室合成溴体的装置示意图及有关数据如下:
(2013?无锡一模)溴苯是一种化工原料,实验室合成溴体的装置示意图及有关数据如下: 溴苯是一种化工原料,实验室合成溴苯的装置示意图如图及有关数据如下:按下列合成步骤回答问题:
溴苯是一种化工原料,实验室合成溴苯的装置示意图如图及有关数据如下:按下列合成步骤回答问题: +Br2
+Br2 +HBr
+HBr