题目内容
【题目】【选做题——物质结构与性质】
早期发现的一种天然二十面体准晶颗粒由 Al、Cu、Fe 三种金属元素组成,回答下列问题:
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过___________方法区分晶体、准晶体和非晶体。
(2)基态Fe原子有个___________个未成对电子。Fe3+的电子排布式为_____________ 。
(3)新制备的Cu(OH)2可将乙醛(CH3CHO)氧化为乙酸,而自身还原成Cu2O。乙醛中碳原子的杂化轨道类型为__________,1 mol乙醛分子中含有的σ键的数目为______________。Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有___________个铜原子。锗也是一种半导体材料,Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键,从原子结构角度分析,原因是_______________________。
(4)如图是金属Ca和D所形成的某种合金的晶胞结构示意图

镧镍合金与上述合金都具有相同类型的晶胞结构XYn,它们有很强的储氢能力。已知镧镍合金LaNin晶胞体积为9.0×10-23 cm3,储氢后形成LaNinH4.5合金(氢进入晶胞空隙,体积不变),则LaNin中n=_____________(填数值);氢在合金中的密度为_____________。
【答案】(1)X射线衍射(1分)(2)4(1分)1s22s22p63s23p63d5或[Ar]3d5 (1分)
(3)sp3、sp2 ,6NA(1分)16 Ge原子半径较大,难以形成稳定的π键,不易形成双键或叁键(4)5;0.083g/cm3
【解析】
试题分析:(1)从外观无法区分三者,但用X光照射挥发现:晶体对X射线发生衍射,非晶体不发生衍射,准晶体介于二者之间,因此通过有无衍射现象即可确定;
(2)26号元素Fe基态原子核外电子排布式为1s22s22p63s23p63d64s2,可知在3d上存在4个未成对电子,失去电子变为铁离子时,先失去4s上的2个电子后失去3d上的1个电子,因此Fe3+的电子排布式为1s22s22p63s23p63d5;
(3)乙醛中甲基上的C形成4个σ键,无孤电子对,因此采取sp3杂化类型,醛基中的C形成3个σ键和1个π键,无孤电子对,采取sp2杂化类型;1个乙醛分子含有6个σ键和一个π键,则1mol乙醛含有6molσ键,即6NA个σ键;该晶胞中O原子数为4×1+6×![]() +8×
+8×![]() =8,由Cu2O中Cu和O的比例可知该晶胞中铜原子数为O原子数的2倍,即为16个;由于Ge原子半径较大,难以形成稳定的π键,因此不易形成双键或叁键。
=8,由Cu2O中Cu和O的比例可知该晶胞中铜原子数为O原子数的2倍,即为16个;由于Ge原子半径较大,难以形成稳定的π键,因此不易形成双键或叁键。
(4)Ca、D合金化学式为CaD5,镧镍合金与上述合金都具有相同类型的晶胞结构XYn,所以该镧镍合金中n=5;该物质密度=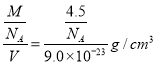 =0.083 g/cm3。
=0.083 g/cm3。

【题目】为了提高煤的利用率,人们先把煤转化为CO和H2,再将它们转化为甲醇,某实验人员在一定温度下的密闭容器中,充入一定量的H2和CO,发生反应:
2H2(g)+CO(g)![]() CH3OH(g),测定的部分实验数据如下:
CH3OH(g),测定的部分实验数据如下:
t/s | 0 | 500 | 1 000 |
c(H2)/(mol·L-1) | 5.00 | 3.52 | 2.48 |
c(CO)/(mol·L-1) | 2.50 |
(1)在500 s内用H2表示的化学反应速率是 。
(2)在1 000 s内用CO表示的化学反应速率是 ,1 000 s时CO的转化率是 。
(3)在500 s时生成的甲醇的浓度是 。
【题目】化学在生产、生活中有广泛应用,下列对应关系正确的是
选项 | 化学性质 | 实际应用 |
A | 碳元素的非金属性比硅强 | 石英和碳粉的混合物高温下反应制备粗硅 |
B | 乙醇能使蛋白质变性 | 无水乙醇作医用消毒剂 |
C | 明矾溶液显酸性 | 明矾作净水剂 |
D | 油脂在碱性条件下水解 | 热的NaOH溶液鉴别植物油和矿物油 |
A. A B. B C. C D. D