题目内容
(1)与CO互为等电子体的分子和离子分别为
(2)H2O的中心原子的价层电子对数为
(3)在CH4、CH3OH中,碳原子采取sp3杂化的分子有
(4)烯烃易发生加成反应的原因
N2
N2
和CN-
CN-
(各举一种即可,填化学式),与NH4+互为等电子体的分子为CH4
CH4
一种即可,填化学式).(2)H2O的中心原子的价层电子对数为
4
4
,VSEPR模型名称为四面体
四面体
,分子的立体结构名称为V形
V形
CO32-的中心原子的价层电子对数为3
3
,VSEPR模型名称为平面三角形
平面三角形
,离子的立体结构名称为平面三角形
平面三角形
CCl4的中心原子的价层电子对数为4
4
,VSEPR模型名称为正四面体
正四面体
,分子的立体结构名称为正四面体
正四面体
.(3)在CH4、CH3OH中,碳原子采取sp3杂化的分子有
CH4、CH3OH
CH4、CH3OH
,SiH4的熔、沸点比CH4高,其主要原因是SiH4比CH4的相对分子质量大,分子间作用力强
SiH4比CH4的相对分子质量大,分子间作用力强
.(4)烯烃易发生加成反应的原因
C=C中的π键,不稳定易断裂
C=C中的π键,不稳定易断裂
,可用苯从溴水中萃取溴的原因溴在苯中的溶解度比在水中要大得多
溴在苯中的溶解度比在水中要大得多
,苯与水互不溶解能分成两层
苯与水互不溶解能分成两层
,苯与溴不会发生反应
苯与溴不会发生反应
.氨气极易溶于水的因氨气是极性键形成的极性分子,水也是极性键形成的极性分子,而且二者之间能形成氢键
氨气是极性键形成的极性分子,水也是极性键形成的极性分子,而且二者之间能形成氢键
.分析:(1)根据等电子体是指具有相同价电子数目和原子数目的分子或离子来回答;
(2)价层电子对数=σ键电子对数+孤电子对数;根据价层电子对数判断VSEPR模型和分子的立体结构;
(3)根据中心原子的价层电子对数判断杂化类型;
(4)C=C中的π键,不稳定易断裂,根据萃取剂的选择原则分析.
(2)价层电子对数=σ键电子对数+孤电子对数;根据价层电子对数判断VSEPR模型和分子的立体结构;
(3)根据中心原子的价层电子对数判断杂化类型;
(4)C=C中的π键,不稳定易断裂,根据萃取剂的选择原则分析.
解答:解:(1)等电子体是指具有相同价电子数目和原子数目的分子或离子,与CO互为等电子体的分子和离子分别为N2、CN-;与NH4+互为等电子体的分子为CH4,
故答案为:N2;CN-;CH4;
(2)价层电子对数=σ键电子对数+孤电子对数,根据水的电子式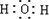 可知,中心原子O有2个孤电子对和2个σ键电子对,共4个价层电子对;VSEPR模型名称为四面体,分子的立体结构名称为V形;CO32-的中心原子的价层电子对数为3;VSEPR模型名称为 平面三角形,离子的立体结构名称为 平面三角形;CCl4的中心原子的价层电子对数为4,VSEPR模型名称为 正四面体,分子的立体结构名称为正四面体,
可知,中心原子O有2个孤电子对和2个σ键电子对,共4个价层电子对;VSEPR模型名称为四面体,分子的立体结构名称为V形;CO32-的中心原子的价层电子对数为3;VSEPR模型名称为 平面三角形,离子的立体结构名称为 平面三角形;CCl4的中心原子的价层电子对数为4,VSEPR模型名称为 正四面体,分子的立体结构名称为正四面体,
故答案为:4;四面体;V形;3;平面三角形;平面三角形;4;正四面体;正四面体;
(3)在CH4、CH3OH中,C原子都是以单键存在,C原子形成了4个σ键,都是sp3杂化,所以碳原子采取sp3杂化的分子有CH4、CH3OH;SiH4比CH4的相对分子质量大,分子间作用力强,所以SiH4的熔、沸点比CH4高,
故答案为:CH4、CH3OH;SiH4比CH4的相对分子质量大,分子间作用力强;
(4)C=C中有一个σ键和一个π键,π键不稳定易断裂,发生加成反应;萃取剂的选择原则:一是溶质在萃取剂中的溶解度比在水中要大得多;二是萃取剂与水互不溶解能分成两层;三是萃取剂与溶质不会发生反应;氨气是极性键形成的极性分子,水也是极性键形成的极性分子,而且二者之间能形成氢键,所以氨气极易溶于水;
故答案为:C=C中的π键,不稳定易断裂;溴在苯中的溶解度比在水中要大得多;苯与水互不溶解能分成两层;苯与溴不会发生反应;氨气是极性键形成的极性分子,水也是极性键形成的极性分子,而且二者之间能形成氢键.
故答案为:N2;CN-;CH4;
(2)价层电子对数=σ键电子对数+孤电子对数,根据水的电子式
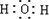 可知,中心原子O有2个孤电子对和2个σ键电子对,共4个价层电子对;VSEPR模型名称为四面体,分子的立体结构名称为V形;CO32-的中心原子的价层电子对数为3;VSEPR模型名称为 平面三角形,离子的立体结构名称为 平面三角形;CCl4的中心原子的价层电子对数为4,VSEPR模型名称为 正四面体,分子的立体结构名称为正四面体,
可知,中心原子O有2个孤电子对和2个σ键电子对,共4个价层电子对;VSEPR模型名称为四面体,分子的立体结构名称为V形;CO32-的中心原子的价层电子对数为3;VSEPR模型名称为 平面三角形,离子的立体结构名称为 平面三角形;CCl4的中心原子的价层电子对数为4,VSEPR模型名称为 正四面体,分子的立体结构名称为正四面体,故答案为:4;四面体;V形;3;平面三角形;平面三角形;4;正四面体;正四面体;
(3)在CH4、CH3OH中,C原子都是以单键存在,C原子形成了4个σ键,都是sp3杂化,所以碳原子采取sp3杂化的分子有CH4、CH3OH;SiH4比CH4的相对分子质量大,分子间作用力强,所以SiH4的熔、沸点比CH4高,
故答案为:CH4、CH3OH;SiH4比CH4的相对分子质量大,分子间作用力强;
(4)C=C中有一个σ键和一个π键,π键不稳定易断裂,发生加成反应;萃取剂的选择原则:一是溶质在萃取剂中的溶解度比在水中要大得多;二是萃取剂与水互不溶解能分成两层;三是萃取剂与溶质不会发生反应;氨气是极性键形成的极性分子,水也是极性键形成的极性分子,而且二者之间能形成氢键,所以氨气极易溶于水;
故答案为:C=C中的π键,不稳定易断裂;溴在苯中的溶解度比在水中要大得多;苯与水互不溶解能分成两层;苯与溴不会发生反应;氨气是极性键形成的极性分子,水也是极性键形成的极性分子,而且二者之间能形成氢键.
点评:本题考查了等电子体、价层电子对数及空间构型的判断、萃取剂选择原则等,题目综合性较强.

练习册系列答案
相关题目
 b
b  c
c 
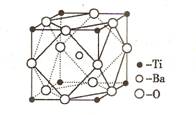
 点如右图,则该化合物的化学式为 ; C、Ni、Mg三种元素中,电负性最大的是 。
点如右图,则该化合物的化学式为 ; C、Ni、Mg三种元素中,电负性最大的是 。

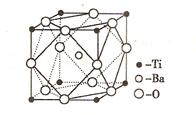
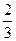 。
。
 。
。 b
b  c
c 

