题目内容
|
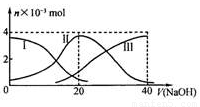
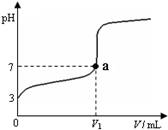
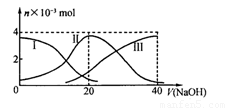
常温下,向20 mL 0.2 mol/L H2A溶液中滴加0.2 mol/L NaOH溶液.有关微粒的物质的量变化如下图(其中I代表H2A,II代表HA-,III代表A2-).根据图示判断,下列说法正确的是
| |
A. |
当V(NaOH)=20 mL时,溶液中离子浓度大小关系:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) |
B. |
等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水的大 |
C. |
NaHA溶液中:c(OH-)+c(A2-)=c(H+)+c(H2A) |
D. |
向Na2A溶液加入水的过程中,pH可能增大也可能减小 |
答案:AC

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目