题目内容
下列说法正确的是(设阿伏加德罗常数的数值为NA)( )
| A、在常温常压下,16g O2和O3的混合气体所含原子数目为NA |
| B、1mol/L K2SO4溶液所含K+数目为2NA |
| C、在标准状况下,22.4L水所含分子数目为NA |
| D、0.1mol Fe与足量稀盐酸完全反应时,转移电子数目为0.3NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.氧气和臭氧中只含有氧原子,16g氧气和臭氧的混合物中含有16g氧原子,含有1mol氧原子;
B.缺少硫酸钾溶液的体积,无法计算溶液中钾离子的数目;
C.标准状况下,水的状态不是气体,不能使用标况下的气体摩尔体积计算水的物质的量;
D.铁与稀盐酸反应生成的是亚铁离子,0.1mol铁完全反应失去0.2mol电子.
B.缺少硫酸钾溶液的体积,无法计算溶液中钾离子的数目;
C.标准状况下,水的状态不是气体,不能使用标况下的气体摩尔体积计算水的物质的量;
D.铁与稀盐酸反应生成的是亚铁离子,0.1mol铁完全反应失去0.2mol电子.
解答:
解:A.16g氧气和臭氧分子中含有16g氧原子,含有1mol氧原子,所含原子数目为NA,故A正确;
B.没有告诉硫酸钾溶液的体积,无法计算溶液中钾离子的数目,故B错误;
C.标况下,水不是气体,不能使用标况下的气体摩尔体积计算22.4L水的物质的量,故C错误;
D.0.1mol铁与足量稀盐酸反应失去0.2mol电子,转移电子数目为0.2NA,故D错误;
故选A.
B.没有告诉硫酸钾溶液的体积,无法计算溶液中钾离子的数目,故B错误;
C.标况下,水不是气体,不能使用标况下的气体摩尔体积计算22.4L水的物质的量,故C错误;
D.0.1mol铁与足量稀盐酸反应失去0.2mol电子,转移电子数目为0.2NA,故D错误;
故选A.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标准状况下乙醇、水、三氧化硫等不是气体,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,选项A为易错点,注意题中缺少溶液的体积.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
观察下列几个装置示意图,有关叙述正确的是( )
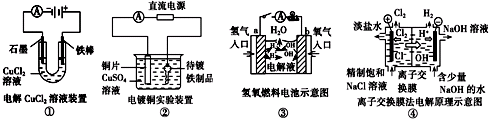

| A、装置①中阳极上析出红色固体 |
| B、装置②的待镀铁制品应与电源负极相连 |
| C、装置③中外电路电子由b极流向a极 |
| D、装置④的离子交换膜允许阳离子、阴离子、水分子自由通过 |
230Th和232Th是90号元素钍的两种同位素,232Th可以转化成233U.下列有关Th的说法正确的是( )
| A、230Th的中子数比核外电子数多140 |
| B、230Th和232Th的化学性质相同 |
| C、232Th转换成233U是化学变化 |
| D、Th元素的相对原子质量是231 |
下列各组离子中,在碱性溶液中能大量共存,且溶液为无色透明的是( )
| A、K+、MnO4-、SO42-、Cl- |
| B、Ca2+、HCO3-、NO3-、SO42- |
| C、K+、NO3-、SO42-、CO32- |
| D、Mg2+、SO42-、CO32-、Cl- |
现有物质的量浓度为0.1mol/L的盐酸和0.1mol/L的氨水,下列说法中正确的是( )
| A、用湿润的pH试纸测定两种溶液的pH时,氨水的误差更大 |
| B、若混合后溶液恰好呈中性时:c(Cl-)=c(NH4+)+c(NH3?H2O) |
| C、两溶液等体积混合时,充分反应后:c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
| D、恰好反应呈中性时,所需氨水的体积大于盐酸的体积 |
在由NaOH、Na2O2组成的化合物中钠元素的质量分数为58%,则混合物中氢元素的质量分数近似为( )
| A、6% | B、2% |
| C、4% | D、无法确定 |
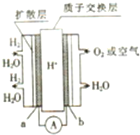 某质子交换膜燃料电池的工作原理如图所示,其中电极a、b均为多孔活性铂电极,下列手法中不正确的是( )
某质子交换膜燃料电池的工作原理如图所示,其中电极a、b均为多孔活性铂电极,下列手法中不正确的是( )| A、a极为该电池的负极 |
| B、该电池的正极反应式为O2+4e-+2H2O=4OH- |
| C、多孔活性铂电极有利于吸附气体,增大接触面积 |
| D、H+(质子)由负极移向正极 |
下面有关硅的叙述中,正确的是( )
| A、光导纤维是以硅酸盐为主要原料制成的 |
| B、硅是构成矿物和岩石的主要元素,硅在地壳中的含量在所有的元素中居第一位 |
| C、硅的化学性质不活泼,在自然界中可以以游离态存在 |
| D、硅在电子工业中,是最重要的半导体材料 |
 A、B、C、D、E、F为中学化学中的常见物质,且物质A由1~2种短周期元素组成,在一定条件下有如下转化关系,请完成下列问题
A、B、C、D、E、F为中学化学中的常见物质,且物质A由1~2种短周期元素组成,在一定条件下有如下转化关系,请完成下列问题