题目内容
【题目】一定温度下,在容积固定的V L密闭容器中加入n mol A、2n mol B,发生反应:
A(g)+2B(g) ![]() 2C(g) ΔH<0,反应达平衡后测得平衡常数为K,此时A的转化率为x。
2C(g) ΔH<0,反应达平衡后测得平衡常数为K,此时A的转化率为x。
(1)一段时间后上述反应达到平衡。则下列说法中正确的是________(填字母)。
A.物质A、B的转化率之比为1∶2
B.起始时刻和达到平衡后容器中的压强之比为3n∶(3n-nx)
C.当2v正(A)=v逆(B)时,反应一定达到平衡状态
D.充入惰性气体(如Ar),平衡向正反应方向移动
(2)K和x的关系满足K=______________。在保证A浓度不变的情况下,扩大容器的体积,平衡________(填字母)。
A.向正反应方向移动
B.向逆反应方向移动
C.不移动
(3)该反应的逆反应速率与时间的关系如图所示。

①由图可知,反应在t1、t3、t7时都达到了平衡,而t2、t8时都改变了一种条件,试判断改变的条件:
t2时____________________________________________________________________;
t8时____________________________________________________________________。
②t2时平衡向________(填“正反应”或“逆反应”)方向移动。
③若t4时降压,t5时达到平衡,t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率与时间的关系线。______
【答案】 BC ![]() C 升温或增大C的浓度 使用催化剂 逆反应
C 升温或增大C的浓度 使用催化剂 逆反应 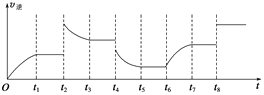
【解析】(1)平衡状态的判断依据是正逆反应速率相等,各组分的浓度保持不变。 A.反应物A与B加入的反应物的物质的量之比等于其化学计量数之比,所以任何时刻A与B的转化率之比等于化学计量数之比为1:2,不能说明达到平衡状态,A错误; B.假设A转化率为x,则平衡后有A、B、C物质的量分别为(n-nx)mol、(2n-2nx)mol、2nxmol,平衡后气体总物质的量为(3n-nx)mol,恒容容器中,气体物质的量之比等于其压强之比,B正确;C.当2v正(A)=v逆(B)时,说明正逆反应速率相等,反应达到平衡状态,C正确;D.恒容容器中,充入惰性气体(如Ar),由于各种物质的浓度不变,所以化学平衡不移动,D错误;答案选BC;(2)在容积固定的V L密闭容器里加入n mol A、2n mol B,发生反应:A(g)+2B(g)![]() 2C(g) △H<0,反应达平衡后测得平衡常数为K,此时A的转化率为x,则化学平衡常数
2C(g) △H<0,反应达平衡后测得平衡常数为K,此时A的转化率为x,则化学平衡常数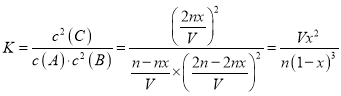 ;增大容器体积时,c(B)和c(C)等比例减小,由于A的浓度不变,此时
;增大容器体积时,c(B)和c(C)等比例减小,由于A的浓度不变,此时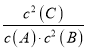 的值仍然等于K,所以平衡不移动,答案选C;(3)①由于纵坐标只表示v逆,t2 时平衡逆向移动,由于该反应的正反应是气体体积减小的放热反应,所以根据平衡移动原理可知,采用的条件可以是升温或增大C的浓度;t8 时正反应速率和逆反应速率都增大,由于二者仍然相等,所以化学平衡不移动,采用的条件是使用了催化剂;②t2 时逆反应速率突然增大,且平衡时反应速率大于t2 时反应速率,平衡向逆反应方向移动;③若t4时降压,物质的浓度降低,反应速率减小,由于反应物的系数大于生成物的稀释,所以正反应速率减小的倍数大于逆反应速率减小的倍数,化学平衡逆向移动,至t5时达到平衡,t6时增大反应物的浓度,化学平衡正向移动,逆反应的速率增大,至t7时达到平衡状态,所以t4~t6时逆反应速率随时间变化的曲线表示为
的值仍然等于K,所以平衡不移动,答案选C;(3)①由于纵坐标只表示v逆,t2 时平衡逆向移动,由于该反应的正反应是气体体积减小的放热反应,所以根据平衡移动原理可知,采用的条件可以是升温或增大C的浓度;t8 时正反应速率和逆反应速率都增大,由于二者仍然相等,所以化学平衡不移动,采用的条件是使用了催化剂;②t2 时逆反应速率突然增大,且平衡时反应速率大于t2 时反应速率,平衡向逆反应方向移动;③若t4时降压,物质的浓度降低,反应速率减小,由于反应物的系数大于生成物的稀释,所以正反应速率减小的倍数大于逆反应速率减小的倍数,化学平衡逆向移动,至t5时达到平衡,t6时增大反应物的浓度,化学平衡正向移动,逆反应的速率增大,至t7时达到平衡状态,所以t4~t6时逆反应速率随时间变化的曲线表示为 。
。

【题目】铁和铝是两种重要的金属,它们的单质及化合物有着各自的性质。
(1)在一定温度下,氧化铁可以与一氧化碳发生反应:Fe2O3(s)+3CO(g) ![]() 2Fe(s)+3CO2(g)。已知该反应在不同温度下的平衡常数如下表:
2Fe(s)+3CO2(g)。已知该反应在不同温度下的平衡常数如下表:
温度/℃ | 1 000 | 1 150 | 1 300 |
平衡常数 | 64.0 | 50.7 | 42.9 |
请回答下列问题:
①该反应的平衡常数表达式K=__________,ΔH____0(填“>”、“<”或“=”)。
②在一个容积为10 L的密闭容器中,1 000 ℃时加入Fe、Fe2O3、CO、CO2各1.0 mol,反应经过10 min后达到平衡。求该时间范围内反应的平均反应速率v(CO2)=________,CO的平衡转化率为________。
③欲提高②中CO的平衡转化率,可采取的措施是_____________________。
A.减少Fe的量 B.增加Fe2O3的量
C.移出部分CO2 D.提高反应温度
E.减小容器的容积 F.加入合适的催化剂
(2)某些金属氧化物粉末和Al粉在镁条的引燃下可以发生铝热反应,下列反应速率(v)和温度(T)的关系示意图中与铝热反应最接近的是________。

(3)写出氢氧化铝在水中发生碱式电离的电离方程式:
_________________________________________________________。
欲使上述体系中Al3+浓度增加,可加入的物质是______________________。
