题目内容
(2009?三明一模)短周期主族元素X、Y、Z、W的原子序数依次增大,其中X、Y、Z位于不同周期,Y是形成化合物种类最多的元素,W2+与Ne原子具有相同的电子层结构.
(1)由X、Y组成的最简单化合物可作某一燃料电池的
(2)Z与氧组成的某种化合物可作为潜水员的供氧剂,该化合物中含有的化学键是
(3)即热饭盒中,有W的单质与铁粉、固体食盐组成混合物A,使用时将水加入A中,几分钟后饭菜变热了.从能量转化角度看,该过程是化学能转化为
(4)500℃时,密闭容器中充入1mol/L CO2和3mol/L H2发生反应:CO2(g)+3H2(g)
CH3OH(g)+H2O(g),测得有关数据如下:
500℃时该反应的平衡常数K=
(5)已知:298K时,Ca(s)=Ca2+(g)+2e-△H=1807kJ/mol
O2(g)++2e-=O2-(g)△H=986kJ/mol
Ca2+(g)+O2-(g)=CaO(s)△H=-3528.5kJ/mol
298K时,金属钙和氧气反应生成CaO固体的热化学方程式为
(1)由X、Y组成的最简单化合物可作某一燃料电池的
负
负
极反应物.(2)Z与氧组成的某种化合物可作为潜水员的供氧剂,该化合物中含有的化学键是
离子键和共价键
离子键和共价键
.(3)即热饭盒中,有W的单质与铁粉、固体食盐组成混合物A,使用时将水加入A中,几分钟后饭菜变热了.从能量转化角度看,该过程是化学能转化为
热
热
能.写出W与水反应的化学方程式:Mg+2H2O
Mg(OH)2+H2↑
| ||
Mg+2H2O
Mg(OH)2+H2↑
.
| ||
(4)500℃时,密闭容器中充入1mol/L CO2和3mol/L H2发生反应:CO2(g)+3H2(g)
| 加热、加压 |
| 催化剂 |
| 反应时间/min | 3 | 5 | 7 | 10 | 13 |
| c(CO2)/mol?L-1 | 0.50 | 0.37 | 0.30 | 0.25 | 0.25 |
5.3
5.3
(保留一痊小数),平衡时CO2的转化率为75%
75%
,温度升高,K值增大,则正反应为吸
吸
热反应(填“吸”或“放”).(5)已知:298K时,Ca(s)=Ca2+(g)+2e-△H=1807kJ/mol
| 1 |
| 2 |
Ca2+(g)+O2-(g)=CaO(s)△H=-3528.5kJ/mol
298K时,金属钙和氧气反应生成CaO固体的热化学方程式为
Ca(s)+
O2(g)=CaO(s)△H=-735.5kJ/mol
| 1 |
| 2 |
Ca(s)+
O2(g)=CaO(s)△H=-735.5kJ/mol
.| 1 |
| 2 |
分析:Y是形成化合物种类最多的元素,应为C元素,对应的化合物种类繁多,X、Y、Z位于不同周期,且X、Y、Z、W的原子序数依次增大,则X应为H元素,Z为第三周期元素,W2+与Ne原子具有相同的电子层结构,应为Mg元素,则Z应为Na元素,
(1)X、Y组成的最简单化合物为CH4;
(2)Z与氧组成的化合物中能作供氧剂的为Na2O2;
(3)Mg和水的反应为放热反应,反应的化学方程式为Mg+2H2O
Mg(OH)2+H2↑;
(4)利用三段式法计算;
(5)利用盖斯定律计算反应热.
(1)X、Y组成的最简单化合物为CH4;
(2)Z与氧组成的化合物中能作供氧剂的为Na2O2;
(3)Mg和水的反应为放热反应,反应的化学方程式为Mg+2H2O
| ||
(4)利用三段式法计算;
(5)利用盖斯定律计算反应热.
解答:解:Y是形成化合物种类最多的元素,应为C元素,对应的化合物种类繁多,X、Y、Z位于不同周期,且X、Y、Z、W的原子序数依次增大,则X应为H元素,Z为第三周期元素,W2+与Ne原子具有相同的电子层结构,应为Mg元素,则Z应为Na元素,则
(1)X、Y组成的最简单化合物为CH4,可被氧化,作原电池的负极,故答案为:负;
(2)Z与氧组成的化合物中能作供氧剂的为Na2O2,为离子化合物,含有离子键和共价键,
故答案为:离子键和共价键;
(3)W的单质与铁粉、固体食盐组成混合物A,使用时将水加入A中,几分钟后饭菜变热了,说明反应为放热反应,在铁粉和食盐的存在条件下发生原电池反应,如是Mg和水反应,则应在加热的条件下才可,反应的化学方程式为
Mg+2H2O
Mg(OH)2+H2↑,
故答案为:热;Mg+2H2O
Mg(OH)2+H2↑;
(4)CO2(g)+3H2(g)
CH3OH(g)+H2O(g)
起始:1mol/L 3mol/L 0 0
转化:0.75mol/L 2.25mol/L 0.75mol/L 0.75mol/L
平衡:0.25mol/L 0.75mol/L 0.75mol/L 0.75mol/L
则k=
=5.3,
平衡时CO2的转化率=
×100%=75%,
温度升高,K值增大,说明平衡向正反应方向移动,则正反应为吸热反应,
故答案为:5.3; 75%; 吸;
(5)已知:①Ca(s)=Ca2+(g)+2e-△H=1807kJ/mol
②
O2(g)++2e-=O2-(g)△H=986kJ/mol
③Ca2+(g)+O2-(g)=CaO(s)△H=-3528.5kJ/mol
利用盖斯定律将①+②+③可得:Ca(s)+
O2(g)=CaO(s),
△H=1807kJ/mol+986kJ/mol+(-735.5 kJ/mol)=-735.5 kJ/mol,
所以热化学方程式为Ca(s)+
O2(g)=CaO(s)△H=-735.5 kJ/mol,
故答案为:Ca(s)+
O2(g)=CaO(s)△H=-735.5 kJ/mol.
(1)X、Y组成的最简单化合物为CH4,可被氧化,作原电池的负极,故答案为:负;
(2)Z与氧组成的化合物中能作供氧剂的为Na2O2,为离子化合物,含有离子键和共价键,
故答案为:离子键和共价键;
(3)W的单质与铁粉、固体食盐组成混合物A,使用时将水加入A中,几分钟后饭菜变热了,说明反应为放热反应,在铁粉和食盐的存在条件下发生原电池反应,如是Mg和水反应,则应在加热的条件下才可,反应的化学方程式为
Mg+2H2O
| ||
故答案为:热;Mg+2H2O
| ||
(4)CO2(g)+3H2(g)
| 加热、加压 |
| 催化剂 |
起始:1mol/L 3mol/L 0 0
转化:0.75mol/L 2.25mol/L 0.75mol/L 0.75mol/L
平衡:0.25mol/L 0.75mol/L 0.75mol/L 0.75mol/L
则k=
| 0.75×0.75 |
| 0.25×0.753 |
平衡时CO2的转化率=
| 0.75 |
| 1 |
温度升高,K值增大,说明平衡向正反应方向移动,则正反应为吸热反应,
故答案为:5.3; 75%; 吸;
(5)已知:①Ca(s)=Ca2+(g)+2e-△H=1807kJ/mol
②
| 1 |
| 2 |
③Ca2+(g)+O2-(g)=CaO(s)△H=-3528.5kJ/mol
利用盖斯定律将①+②+③可得:Ca(s)+
| 1 |
| 2 |
△H=1807kJ/mol+986kJ/mol+(-735.5 kJ/mol)=-735.5 kJ/mol,
所以热化学方程式为Ca(s)+
| 1 |
| 2 |
故答案为:Ca(s)+
| 1 |
| 2 |
点评:本题考查元素的推断,推断部分难度不大,本题侧重于化学平衡和化学反应与能量的考查,特别是化学平衡的计算依据盖斯定律的应用,为该题的难点同时也是化学反应原理模块考查的重点内容学习中要注重相关知识、方法的积累和把握.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
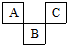 (2009?三明一模)A、B、C三种短周期元素在周期表中位置如图示,B位于ⅥA族.下列叙述错误的是( )
(2009?三明一模)A、B、C三种短周期元素在周期表中位置如图示,B位于ⅥA族.下列叙述错误的是( )